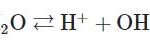Tính chất hóa học của axit và các dạng bài tập liên quan chuẩn 100%
Cùng với muối, bazơ và oxit, axit là một trong những hợp chất hóa học cơ bản mà các em sẽ được học trong môn Hóa từ bậc trung học cơ sở cho đến trung học phổ thông. Vậy axit là gì? Tính chất tính chất hóa học của axit là gì? Vì vậy hôm nay chúng tôi sẽ giúp các em giải đáp những câu hỏi này qua bài viết dưới đây.
Tham khảo thêm:
- Tính chất hóa học của nước và các dạng bài tập liên quan chuẩn 100%
- Hiệu Suất là gì ? Công thức tính hiệu suất phản ứng hóa học
- Công thức tính nồng độ mol, số mol và C nồng độ phần trăm
Nội Dung
Axit là gì?
Axit là một hợp chất hóa học có công thức HxA, có vị chua và tan được trong nước để tạo ra dung dịch có nồng độ pH < 7. Độ pH càng lớn thì tính axit càng yếu và ngược lại.
Ngoài ra, còn một cách định nghĩa axit là gì khác như sau “Axit là các phân tử hay ion có khả năng nhường proton H+ cho bazo hoặc nhận các cặp electron không chia từ bazo”.
Phân loại axit
Dựa vào tính chất hóa học của axit
+) Axit mạnh: Axit clohydric HCl, axit sulfuric H2SO4, axit nitric HNO3,…
+) Axit yếu: Hydro sunfua H2S, axit cacbonic H2CO3,…
Dựa vào nguyên tử oxy
+) Axit không có oxi: HCl, H2S, HBr, HI, HF…
+) Axit có oxi: H2SO4, HNO3, H3PO4, H2CO3…
Ngoài ra, ta còn có thể phân chia axit theo như các dạng dưới đây:
+) Axit vô cơ: HCl, H2SO4, HNO3,…
+) Axit hữu cơ – RCOOH: CH3COOH, HCOOH,…
Cách xác định độ mạnh, yếu của axit
+) Dựa vào sự linh động của nguyên tử Hydro trong axit đó. Nếu H càng linh động, tính axit càng mạnh và ngược lại.
+) Với những axit có oxy trong cùng một nguyên tố, càng ít oxy, axit càng yếu
HClO4 > HClO3> HClO2> HClO
+) Với những axit của nguyên tố trong cùng chu kỳ, khi các nguyên tố ở hóa trị cao nhất, nguyên tố trung tâm có tính phi kim càng yếu thì axit đó càng yếu.
HClO4> H2SO4> H3PO4
+) Với axit của nguyên tố cùng nhóm A
- Axit có oxy: Tính axit tăng dần từ dưới lên: HIO4 < HbrO4< HClO4
- Axit không có oxy: Tính axit giảm dần từ dưới lên: HI > HBr> HCl> HF
+) Với axit hữu cơ RCOOH
- Nếu R đẩy electron (gốc R no) thì tính axit giảm
- HCOOH> CH3COOH> CH3CH2COOH> CH3CH2CH2COOH> n-C4H9COOH.
- Nếu R hút e (gốc R không no, thơm hoặc có nguyên tố halogen,…), tính axit sẽ mạnh
Tính chất hóa học của axit
Axit làm đổi màu chất chỉ thị màu
+) Dung dịch axit làm đổi màu quỳ tím thành đỏ.
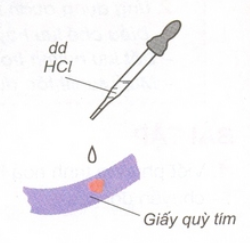
+) Trong hóa học, quỳ tím là chất chỉ thị màu để nhận biết dung dịch axit.
Axit tác dụng với kim loại
+) Dung dịch axit tác dụng được với nhiều kim loại tạo thành muối và giải phóng khí hiđro.
Ví dụ:
3H2SO4 (dd loãng) + 2Al → Al2(SO4)3 + 3H2 (↑)
2HCl + Fe → FeCl2 + H2 (↑)
+) Các kim loại Hg, Cu, Ag, Au, Pt …không tác dụng với HCl, H2SO4 loãng.
Chú ý: Axit HNO3 và H2SO4 đặc tác dụng được với nhiều kim loại nhưng không giải phóng khí hiđro.
Axit tác dụng với bazơ
Axit + bazơ → muối + H2O
Ví dụ:
H2SO4 + Cu(OH)2 → CuSO4 + 2H2O
HCl + NaOH → NaCl + H2O
Phản ứng của axit với bazơ được gọi là phản ứng trung hòa.
Axit tác dụng với oxit bazơ
Axit + oxit bazơ → muối + H2O
Ví dụ:
6HCl + Fe2O3 → FeCl3 + 3H2O
H2SO4 + MgO → MgSO4 + H2O
Ngoài ra, axit còn tác dụng với muối.
Ví dụ:
MgCO3 + 2HCl → MgCl2 + CO2 ↑ + H2O
Na2SO3 + 2HCl → 2NaCl + SO2 ↑ + H2O
Các dạng bài tập áp dụng tính chất hóa học của axit thường gặp
Bài 1: Từ Mg, MgO, Mg(OH)2 và dung dịch axit sunfuric loãng, hãy viết các phương trình phản ứng hóa học điều chế magie sunfat.
Giải:
Phương trình hóa học:
Mg + H2SO4(loãng) → MgSO4 + H2
MgO + H2SO4 → MgSO4 + H2O
Mg(OH)2 + H2SO4 → MgSO4 + 2H2O
Bài 2: Có những chất sau: CuO, Mg, Al2O3, Fe(OH)3, Fe2O3. Hãy chọn một trong những chất đã cho tác dụng với dung dịch HCl sinh ra:
a) Khí nhẹ hơn không khí và cháy được trong không khí.
b) Dung dịch có màu xanh lam.
c) Dung dịch có màu vàng nâu.
d) Dung dịch không có màu.
Viết các phương trình phản ứng.
Giải:
a) Khí nhẹ hơn không khí và cháy được trong không khí là khí H2.
Mg + 2HCl → MgCl2 + H2 ↑
b) Dung dịch có màu xanh lam là dung dịch CuCl2.
CuO + 2HCl → CuCl2 + H2O
c) Dung dịch có màu vàng nâu là dung dịch FeCl3.
Fe(OH)3 + 3HCl → FeCl3 + 3H2O
Hoặc Fe2O3 + 6HCl → 2FeCl3 + 3H2O
d) Dung dịch không màu là các dung dịch MgCl2, AlCl3.
Al2O3 + 6HCl → 2AlCl3 + 3H2O
Mg + 2HCl → MgCl2 + H2 ↑
Bài 3: Hãy viết các phương trình phản ứng trong mỗi trường hợp sau:
a) Magie oxit và axit nitric.
b) Đồng (II) oxit và axit clohiđric.
c) Nhôm oxit và axit sunfuric.
d) Sắt và axit clohiđric.
e) Kẽm và axit sunfuric loãng.
Giải:
Phương trình hóa học của các phản ứng:
a) MgO + 2HNO3 → Mg(NO3)2 + H2O
b) CuO + 2HCl → CuCl2 + H2O
c) Al2O3 + 3H2SO4 → Al2(SO4)3 + 3H2O
d) Fe + 2HCl → FeCl2 + H2 ↑
e) Zn + H2SO4(loãng) → ZnSO4 + H2 ↑ .
Bài 4: Có 10g hỗn hợp bột các kim loại đồng và sắt. Hãy giới thiệu phương pháp xác định thành phần phần trăm (theo khối lượng) của mỗi kim loại trong hỗn hợp theo:
a) Phương pháp hóa học. Viết phương trình hóa học.
b) Phương pháp vật lí.
Giải:
a) Phương pháp hóa học:
– Ngâm hỗn hợp Cu và Fe trong dung dịch HCl dư.
– Phản ứng xong, lọc lấy chất rắn, rửa nhiều lần trên giấy lọc.
– Làm khô chất rắn, thu được bột Cu.
– Cân, giả sử ta cân được 7,2g. Từ đó suy ra trong hỗn hợp có 7,2g Cu và 10-7,2= 2,8g Fe
⇒ % Cu = (7,2/10).100% = 72% và % Fe = 100% – 72% = 28%
PTHH: Fe + 2HCl → FeCl2 + H2↑
Cu + HCl → không phản ứng.
b) Phương pháp vật lí:
Dùng thanh nam châm, sau khi đã bọc đầu nam châm bằng mảnh nilon mỏng và nhỏ. Chà nhiều lần trên hỗn hợp bột ta cũng thu được 2,8g bột Fe.
Bài 5: MgCO3 tác dụng với dung dịch HCl sinh ra:
Giải:
MgCO3 + 2HCl → MgCl2 + CO2 ↑ + H2O
CO2 là khí không cháy, không duy trì sự cháy, sư sống.
Khí CO2 tan ít trong nước và làm đục nước vôi trong theo phản ứng:
CO2 + Ca(OH)2 → CaCO3↓ + H2O
Bài 6: Cho 4,8 gam kim loại magie tác dụng vừa đủ với dung dịch axit sunfuric loãng. Thể tích khí Hiđro thu được ở đktc là:
Giải:
nMg = 4,8 : 24 = 0,2 mol
Mg + H2SO4 → MgSO4 + H2 ↑
0,2 0,2 mol
→ Vkhí = 0,2.22,4 = 4,48 lít.
Mong rằng những nội dung trên đây sẽ giúp bạn trả lời được những thắc mắc câu hỏi của mình. Hơn hết đó là có thể giải được những bài toán của mình