Ancol là gì? Tính chất hóa học, công thức, cách điều chế ancol và các dạng bài tập
Ancol là gì? Công thức của ancol là gì? Ancol có đặc điểm tính chất lý hóa như thế nào? Cách điều chế và ứng dụng của ancol ra sao? Cùng chúng tôi giải đáp những vấn đề này nhé.
Tham khảo thêm:
- Phản ứng hóa học là gì? Khi nào phản ứng hóa học xảy ra và các dạng bài tập
- Dãy Điện Hóa là gì ? Cách đọc Dãy Điện Hõa kim loại dễ thuộc
- Bảng hóa trị của các nguyên tố và cách học thuộc bằng bài ca hóa trị
Nội Dung
Ancol là gì?
Ancol là những hợp chất hữu cơ mà phân tử có nhóm hidroxyl (OH) liên kết trực tiếp với nguyên tử cacbon no.
+) Công thức tổng quát của ancol: R(OH)n (n ≥ 1), với R là gốc hiđrocacbon.
+) Công thức của ancol no mạch thẳng, đơn chức: CnH2n+1OH hay CnH2n+2O (với n ≥ 1).
Phân loại ancol
Gốc R có thể là mạch hở no hay chưa no hoặc mạch vòng.
Ví dụ: CH3-OH; CH2=CH-CH2-OH; C6H5-CH2-OH.
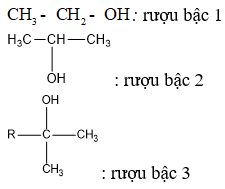
Nhóm OH- có thể dính vào cacbon bậc 1, bậc 2, bậc 3 tạo thành ancol tương ứng bậc 1, bậc 2, bậc 3.
Lưu ý: Bậc của ancol bằng bậc của nguyên tử cacbon liên kết với nhóm OH.
Ví dụ:
Bảng phân loại ancol:
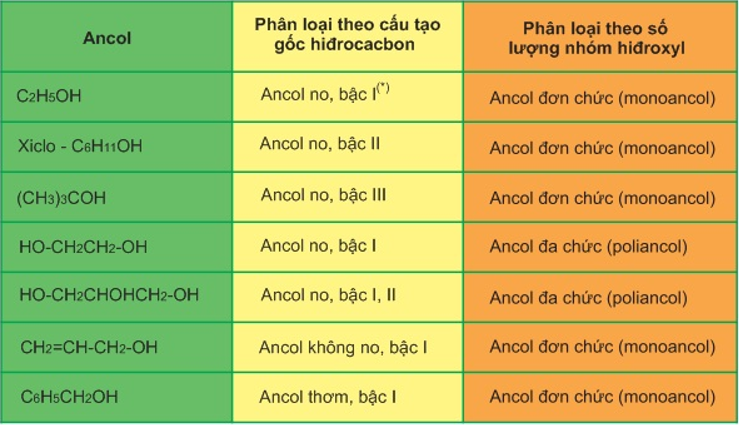
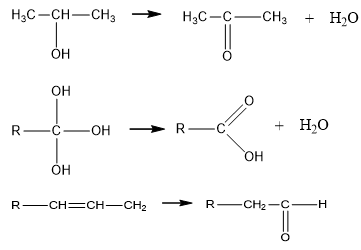
Ancol không bền khi:
- Nhiều nhóm –OH cùng đính vào một nguyên tử cacbon.
- Nhóm –OH đính vào nguyên tử cacbon có nối đôi.
Ví dụ:
Đồng phân và danh pháp
Đồng phân:
- Mạch cacbon khác nhau.
- Vị trí của các nhóm –OH khác nhau.
- Ngoài ra ancol đơn chức có đồng phân là ete: R-O-R’.
Ví dụ: Viết đồng phân của C3H8O.
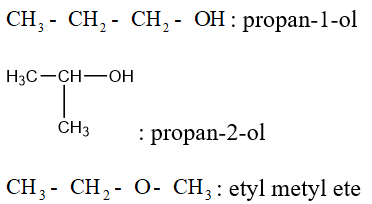
Danh pháp:
Tên thông thường: Tên ancol = tên gốc hiđrocacbon no tương ứng + ic.
Ví dụ:
CH3-CH2-OH: ancol etylic.
CH3-OH: ancol metylic.
Tên thay thế: Tên ancol = tên gốc hiđrocacbon no tương ứng + ol.
Ví dụ:
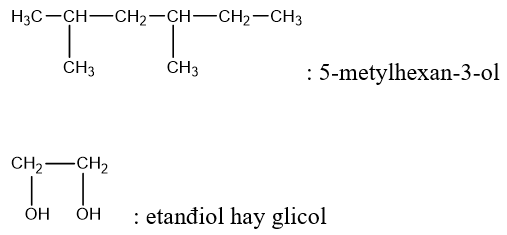
Tính chất vật lý
Các ancol có nhiệt độ sôi cao hơn các hiđcacbon có cùng phân tử khối hoặc đồng phân ete của nó là do giữa các phân tử ancol có liên kết hiđro → Ảnh hưởng đến độ tan.
- Từ C1 đến C12 ancol ở thể lỏng (khối lượng riêng d < 1), từ C13 trở lên ở thể rắn.
- C1 đến C3 tan vô hạn trong nước vì có liên kiết H với nước.
- Độ rượu = (Vancol nguyên chất/Vdd ancol).100
- Các poli như etylen glicol, glixerol thường sánh, nặng hơn nước và có vị ngọt.
Tính chất hóa học
1. Phản ứng thế nguyên tử hiđro của nhóm OH ancol (phản ứng đặc trưng của Ancol)
+) Tính chất chung của ancol:
2ROH + Na → 2RONa + H2↑
+)Tính chất đặc trưng của glixerol:
2C3H5(OH)3 + Cu(OH)2 → [C3H5(OH)2O]2Cu + H2O
(ĐK: muốn tác dụng với Cu(OH)2 phải có 2 nhóm -OH trở lên liền kề nhau)
→ Phản ứng này dùng để phân biệt ancol đơn chức với ancol đa chức có 2 nhóm OH cạnh nhau trong phân tử.
2. Phản ứng thế nhóm OH
+) Phản ứng với axit vô cơ:
![]()
+) Phản ứng tạo dien: dùng sản xuất cao su buna.
![]()
(ĐK: phải có xúc tác là Al2O3 + MgO hoặc ZnO/500ºC)
3. Phản ứng tách nước (phản ứng đêhidrat hoá)
Chú ý:
![]()
(ĐK n ≥ 2, theo quy tắc Zai-xép)
(ancol bậc càng cao thì càng dễ khử nước tạo anken)
![]()
(phải là rượu no, đơn chức)
![]()
(ancol bậc càng thấp thì càng dễ khử nước tạo ete)
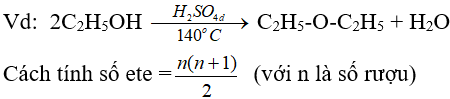
4. Phản ứng oxi hoá
+) Phản ứng oxi hoá hoàn toàn:
![]()
+) Phản ứng oxi hoá không hoàn toàn:
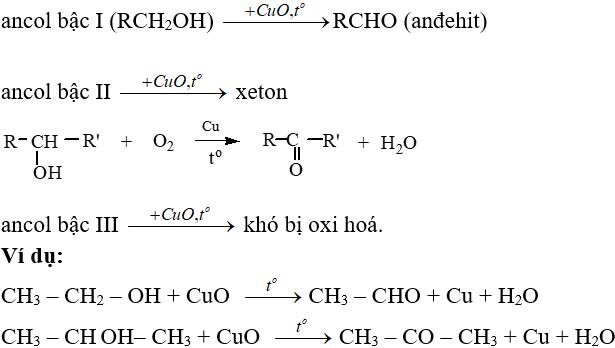
Cách điều chế ancol
+) Thực hiện dẫn xuất halogen
CnH2n+2-2k-xXx + xMOH → CnH2n+2-2k-x(OH)x + xMX
+) Cộng nước vào anken để tạo ra ancol no, đơn chức và mạch hở. Phản ứng được tuân theo quy tắc cộng Maccopnhicop nên nếu anken là đối xứng thì phản ứng chỉ tạo ra 1 ancol
CnH2n + H2O → CnH2n+1OH(H+)
+) Trong môi trường kiềm tiến hành thủy phân este
RCOOR’ + NaOH → RCOONa + R’OH
+) Cộng H2 vào andehit hay xeton
RCHO + H2 → RCH2OH (Ni, to)
RCOR’ + H2 → RCHOHR’ (Ni, to)
+) Dùng dung dịch KMnO4 oxi hóa hợp chất có nối đôi
3CH2=CH2 + 2KMnO4 + 4H2O → 3CH2OH-CH2OH + 2KOH + 2MnO2
Cách ứng dụng của ancol
Metanol được sử dụng chủ yếu trong sản xuất anđehit fomic – nguyên liệu cho ngành công nghiệp chất dẻo
Etanol được dùng để điều chế một số hợp chất hữu cơ như axit axetic, etyl axetat, dietyl ete,… do có khả năng hòa tan tốt một số hợp chất hữu cơ nên chất này được sử dụng trong pha vecni, dược phẩm hay nước hoa,… Trong đời sống, chúng được dùng cho pha chế các loại đồ uống với các độ ancol khác nhau.
Một số bài tập vận dụng về ancol
Bài tập 1: Viết phương trình của phản ứng propan-1-ol với từng chất dưới đây và chỉ ra vai trò của ancol trong đó.
a) Natri kim loại
b) CuO, đun nóng
c) Axit HBr, có xúc tác
Lời giải:
a) 2CH3-CH2-CH2OH + 2Na → 2CH3-CH2-CH2ONa + H2
Ancol làm chất oxi hóa
b) CH3-CH2-CH2OH + CuO → CH3-CH2-CHO + Cu + H2O
Ancol giữ vai trò là chất khử
c) CH3-CH2-CH2OH + HBr → CH3-CH2-CH2Br + H2O
Ancol đóng vai trò là bazơ
Bài tập 2: dùng phương pháp hóa học để phân biệt các chất lỏng etanol, glixerol, nước và benzen trong các lọ không dán nhãn.
Lời giải:
Lấy mỗi chất lỏng 1 ít cho ra các ống nghiệm khác nhau và đánh số thứ tự tương ứng với sản phẩm
Cho lần lượt nước dư vào trong các ống nghiệm
Ống nghiệm nào không tan và có hiện tượng dung dịch phân thành 2 lớp thì là benzen
Với những ống nghiệm còn lại sẽ có hiện tượng đồng nhất
Tiến hàng cho Cu(OH)2 vào 3 chất chưa được xác định, chất cho ra phức màu xanh lam là C3H5(OH)3, còn lại không có hiện tượng gì.
2C3H5(OH3 + Cu(OH)2 → [C3H5(OH)2O]2Cu + 2H2O
Đốt 2 chất còn lại, sau đó cho đi qua dung dịch nước vôi trong, chất nào có sản phẩm sinh ra làm đục nước vôi trong là C2H5OH, còn lại là H2O
C2H5OH + 3O2 → 2CO2 + 3H2O
CO2 + Ca(OH)2 → CaCO3 + H2O
Bài tập 3: cho 3,70 gam một ancol X no, đơn chức và mạch hở tác dụng cùng Na dư có thấy 0,56 lít khí thoát ra ngoài (tại đktc). Vậy công thức phân tử X là:
- C2H6O
- C3H10O
- C4H10O
- C4H8O
Lời giải:
Ta có phương trình phản ứng:
2R-OH + 2Na → 2R-ONa + H2
0,05mol 0,025mol
Theo bài ra ta có: nH2 = 0,56/22,4 = 0,025 mol
Từ PTPƯ: nR-OH = 2.nH2 = 2.0,025 = 0,05 mol
Ta được: MROH = 3,7 : 0,05 = 74 g/mol
=> Ancol no, đơn chức có công thức là CnH2n + 1OH
=> 14n + 8 = 74 => n=4
Vậy đáp án đúng là C: C4H10O
Mong rằng những nội dung trên đây sẽ giúp bạn trả lời được những thắc mắc câu hỏi của mình. Hơn hết đó là có thể giải được những bài toán của mình