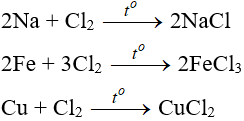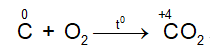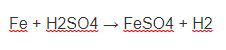Tính chất của phi kim và các dạng bài tập liên quan chuẩn 100%
Ở chương trình Hóa cấp 3, phi kim có rất nhiều chất khác nhau. Đây cũng là lý thuyết quan trọng xuất hiện nhiều trong các bài kiểm tra và bài thi. Nhằm giúp các em nắm vững kiến thức về phi kim, Thpt Chuyên Lam Sơn đã biên soạn và chia sẻ đến các em những lý thuyết trọng tâm bao gồm phi kim là gì, tính chất vật lý, tính chất hóa học của phi kim và một số bài tập vận dụng có đáp án trong bài viết dưới đây.
Tham khảo thêm:
- Tính chất hóa học của cacbon và các dạng bài tập liên quan chuẩn 100%
- Tính chất hóa học của muối và các dạng bài tập liên quan chuẩn 100%
- Tính chất hóa học của clo và các dạng bài tập liên quan chuẩn 100%
Nội Dung
Phi kim là gì?
Phi kim là các nguyên tố hóa học dễ nhận electron nhưng ngoại trừ hidro. Trong cấu trúc sắp xếp ở bảng tuần hoàn thì phi kim là những nguyên tố nằm bên phải bảng tuần hoàn. Nắm được các đặc điểm trên, chúng ta dễ dàng nhận biết được phi kim trong bảng tuần hoàn hóa học cũng như một phần phác họa được tính chất của phi kim.
Tính chất vật lý và hóa học của phi kim
Tính chất vật lí
Ở điều kiện thường, phi kim tồn tại ở cả ba trạng thái: trạng thái rắn như lưu huỳnh, cacbon, photpho … ; trạng thái lỏng như brom; trạng thái khí như oxi, nitơ, hiđro, clo …
Phần lớn các nguyên tố phi kim không dẫn được điện, dẫn nhiệt và có nhiệt độ nóng chảy thấp. Một số phi kim độc như clo, brom, iot.
Tính chất hóa học
+) Tác dụng với kim loại
– Nhiều phi kim tác dụng với kim loại tạo thành muối:

+) Tác dụng với hiđro
Oxi tác dụng với hiđro
+ Khí oxi tác dụng với hiđro tạo thành hơi nước:
![]()
Clo tác dụng với hiđro
+ Hiđro cháy trong khí clo tạo thành khí không màu. Màu vàng lục của khí clo biến mất. Giấy quỳ tím hóa đỏ.
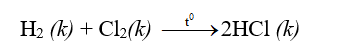
+ Khí clo đã phản ứng mạnh với hiđro tạo thành khí hiđro clorua không màu. Khí này tan trong nước tạo thành dung dịch axit clohiđric và làm quỳ tím hóa đỏ.
– Ngoài ra, nhiều phi kim khác như C, S, Br2,… tác dụng với hiđro cũng tạo thành hợp chất khí.
=>Phi kim phản ứng với hiđro tạo thành hợp chất khí.
+)Tác dụng với oxi
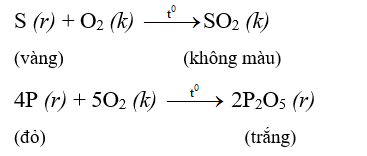
=>Nhiều phi kim tác dụng với oxi tạo thành oxit axit.
+) Mức độ hóa học của phi kim
Mức độ hoạt động hóa học mạnh hay yếu của phi kim được căn cứ vào khả năng và mức độ phản ứng của phi kim đó với kim loại và hiđro. Flo, oxi, clo là những phi kim hoạt động mạnh, flo là phi kim mạnh nhất. Lưu huỳnh, photpho, cacbon, silic là những phi kim hoạt động yếu hơn.
Các dạng bài tập áp dụng tính chất của phi kim thường gặp
Bài 1: Cho sơ đồ biểu diễn chuyển đổi sau:
Phi kim → oxit axit → oxit axit → axit → muối sunfat tan → muối sunfat không tan.
a) Tìm công thức các chất thích hợp để thay cho tên chất trong sơ đồ.
b) Viết các phương trình hóa học biểu diễn chuyển hóa trên.
Giải:
a) Sơ đồ phản ứng:
S → SO2 → SO3 → H2SO4 → Na2SO4 → BaSO4.
b) Phương trình phản ứng:
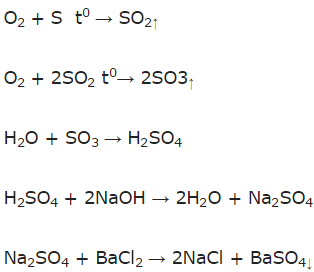
Bài 2: Viết các phương trình hóa học của S, C, Cu, Zn vơí khí O2. Cho biết các oxit tạo thành thuộc loại nào. Vết công thức các axit hoặc bazơ tương ứng với mỗi oxit đó.
Giải:
Phương trình hóa học:
a) S + O2 → SO2 (to)
b) C + O2 → CO2
c) 2Cu + O2 → 2CuO
d) 2Zn + O2 → 2ZnO
Oxit tạo thành là oxit axit:
SO2 axit tương ứng là H2SO3.
CO2 axit tương ứng là H2CO3.
Oxit tạo thành là oxit bazơ :
CuO bazơ tương ứng là Cu(OH)2.
ZnO là oxit lưỡng tính; bazơ tương ứng là Zn(OH)2, axit tương ứng: H2ZnO2
Bài 3: Viết phương trình hóa học khi cho hiđro phản ứng với:
a) clo.
b) lưu huỳnh.
c) brom.
Cho biết trạng thái các chất tạo thành.
Giải:
Phương trình hóa học:
a) H2 (k) + Cl2 (k) → 2HCl(k) (HCl ở trạng thái khí, không màu)
b) S + H2 (k) → H2S (k) (H2S ở trạng thái khí, không màu, có mùi trứng thối)
c) H2 + Br2 → 2HBr(to) (HBr ở trạng thái khí, không màu)
Bài 4:Viết các phương trình hóa học giữa cặp chất sau đây (ghi rõ điều kiện, nếu có):
a) Khí flo và hiđro.
b) Lưu huỳnh và oxi.
c) Bọt sắt và bột lưu huỳnh.
d) Cacbon và oxi.
e) Khí hiđro và lưu huỳnh.
Giải:
Phương trình hóa học:
a) H2 + F2 → 2HF (k)
b) S + O2 → SO2(to)
c) Fe + S → FeS (to).
d) C + O2 → CO2(to).
e) H2 + S → H2S.(to)
Bài 5: Nung hỗn hợp gồm 5,6g sắt và 1,6g lưu huỳnh trong môi trường không có không khí thu được hỗn hợp chất rắn A. Cho dung dịch HCl 1M phản ứng vừa đủ với A thu được hỗn hợp khí B.
a) Hãy viết các phương trình hóa học.
b) Tính thể tích dung dịch HCl 1M đã tham gia phản ứng.
Giải:
nFe = 0,1 mol; nS = 0,05 mol
a) Phương trình phản ứng:
Fe + S → FeS (1)
Theo pt: nFe pư = nS = 0,05 mol ⇒ nFe dư = 0,1 – 0,05 = 0,05mol
nFeS = nS = 0,05 mol
Nên hỗn hợp chất rắn A có Fe dư và FeS
Fe + 2HCl → FeCl2 + H2 ↑ (2)
FeS + 2HCl → FeCl2 + H2S ↑ (3)
b) Dựa vào phương trình phản ứng (2) và (3), ta có:
nHCl = 2.nFe + 2.nFeS = 2. 0,05 + 2. 0,05 = 0,2 mol
VHCl = 0,2 /1 = 0,2 lít.
Bài 6: Viết các phương trình phản ứng theo chuỗi biến hóa sau:
a. Cl2 → NaCl → HCl → CuCl2 →AgCl
b. Cl2 → HCl → AgCl → Cl2 → Br2 →I2
c. MnO2 → Cl2 → KCl → HCl → Cl2 → CaOCl2
Giải:
a. Cl2 + 2Na → 2NaCl
2NaCl + H2SO4 đ → Na2SO4 + 2HCl
2HCl + CuO →CuCl2 + H2O
2CuCl2 + 2AgNO3 → Cu(NO3)2 + 2AgCl↓
b. Cl2 + H2 −a/s→ 2HCl
HCl + AgNO3 → AgCl↓ + HNO3
2AgCl −đ/p→ 2Ag ↓ + Cl2
Cl2 + 2NaBr →2NaCl + Br2
Br2+ 2NaI → 2NaBr + I2
c. MnO2 + 4HCl → MnCl2 + 2H2O + Cl2
Cl2 + 2K → 2KCl
2KCl + H2SO4 đ,n → K2SO4 + 2HCl↑
6HCl + KClO3 → KCl + 3H2O + 3Cl2 ↑
Cl2 + Ca(OH)2 → CaOCl2 + H2O
Bài 2: Bổ túc và cân bằng các pt theo sơ đồ:
a. HCl + ? → Cl2 + ? + ? b. ? + ? →CuCl2 + ?
c. HCl + ? →CO2 + ? + ? d. HCl + ? →AgCl + ?
e. KCl + ? →KOH + ? + ? f. Cl2 + ? →HClO + ?
g. Cl2 + ? NaClO + ? + ? h. Cl2 + ? → CaOCl2 + ?
i. CaOCl2 + ? → HClO + ? k. NaClO + ? → NaHCO3 + ?
Giải:
a. HCl + MnO2 → Cl2 + H2O + MnCl2
b. CuO + HCl → CuCl2 + H2O
c. HCl + Na2CO3 → CO2 + NaCl + H2O
d. HCl + AgNO3 → AgCl ↓ + HNO3
e. KCl + H2O −đpdd cmn→ KOH + Cl2 + H2O
f. Cl2 + H2O → HClO + HCl
g. Cl2 + NaOH → NaClO + NaCl + H2O
h. Cl2 + Ca(OH)2 đặc → CaOCl2 + H2O
i. CaOCl2 + HCl → HClO + CaCl2
k. NaClO + H2CO3 → NaHCO3 + HClO
Mong rằng những nội dung trên đây sẽ giúp bạn trả lời được những thắc mắc câu hỏi của mình. Hơn hết đó là có thể giải được những bài toán của mình