Lý thuyết Mg + HNO3 → Mg(NO3)2 + NH4NO3 + H2O và bài tập có đáp án
Mg + HNO3 → Mg(NO3)2 + NH4NO3 + H2O là phương trình phản ứng oxi hóa khử Mg tác dụng HNO3 sản phẩm khử sinh ra NH4NO3. Sau đây, TPHT Chuyên Lam Sơn hướng dẫn các bạn viết phương trình và cân bằng phản ứng kèm theo các dạng bài tập chi tiết trong bài viết dưới đây
Tham khảo thêm:
Nội Dung
Phương trình phản ứng Mg tác dụng HNO3 loãng:
3Mg + 8HNO3 → 3Mg(NO3)2 + 2NO + 4H2O
Điều kiện phản ứng Mg + HN03: Dung dịch HNO3 loãng dư.
Cách thực hiện phản ứng Mg + HN03: Cho kim loại magie tác dụng với dung dịch axit nitric
Hiện tượng nhận biết phản ứng Mg + HN03: Kim loại tan dần tạo thành dung dịch không màu và khí không màu thoát ra.
Cân bằng phương trình Mg + HNO3→ Mg(NO3)2 + NO + H2O bằng phương pháp cân bằng electron:
Mg0 + HN+5O3 → Mg+2(NO3)2 + N+2O ↑ + H2O
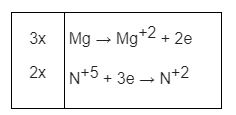
3Mg + 2HNO3 → 3Mg(NO3)2 + 2NO + H2O
Sau đó thêm 6 gốc NO3– (trong đó N không thay đổi số oxi hóa) nghĩa là tất cả có 8HNO3
Cuối cùng ta có:
3Mg + 8HNO3 → 3Mg(NO3)2 + 2NO + 4H2O
Các bước cân bằng phản ứng oxi hoá – khử theo phương pháp thăng bằng electron
Bước 1: Xác định số oxi hoá của những nguyên tố thay đổi số oxi hoá.
Bước 2: Viết quá trình oxi hoá và quá trình khử, cân bằng mỗi quá trình:
- Dấu “+e” đặt bên có số oxi hoá lớn.
- Số e = số oxi hoá lớn – số oxi hoá bé.
- Nhân cả quá trình với chỉ số của nguyên tố thay đổi số oxi hoá nếu chỉ số khác 1 (với các đơn chất có thể chấp nhận giữ nguyên chỉ số).
Bước 3. Tìm hệ số thích hợp sao cho tổng số e cho bằng tổng số e nhận:
- Tìm bội chung nhỏ nhất của số e nhường và nhận.
- Lấy bội chung nhỏ nhất chia cho số e ở từng quá trình được hệ số.
Bước 4. Đặt hệ số của chất oxi hoá và chất khử vào sơ đồ phản ứng và kiểm tra lại.
Phương trình ion thu gọn của Mg + HNO3 loãng
Phương trình ion
3Mg + 8H+ + 5NO3– → 3Mg2+ + 3NO3– + 2NO + 4H2O
Phương trình ion thu gọn:
3Mg + 8H+ + 5NO3− → 3Mg2+ + NO + 4H2O
Axit Nitric tác dụng với kim loại
Axit nitric tác dụng với kim loại trừ Au và Pt tạo muối và nhiều sản phẩm oxi hóa khác nhau như NO2, NO, N2O ,N2, NH4NO3
Sản phẩm khử của N+5 sinh ra tùy thuộc vào độ mạnh yếu của kim loại và nồng độ của dung dịch axit, thông thường thì:
Dung dịch HNO3 đặc tác dụng với kim loại → NO2;
Dung dịch HNO3 loãng tác dụng với kim loại khử yếu (như: Cu, Pb, Ag,..) → NO;
Dung dịch HNO3 loãng tác dụng với kim loại mạnh (như: Al, Mg, Zn,…) thì N bị khử xuống mức càng sâu → (N2, N2O, NH4NO3).
Cách phân biệt các khí sản phẩm sinh ra N2O là khí gây cười
N2 không duy trì sự sống, sự cháy NO2 có màu nâu đỏ
NO khí không màu nhưng bị oxit hóa thành NO2 màu nâu đỏ
NH4NO3 không sinh ra ở dạng khí, khi cho kiềm vào kim loại thấy có mùi khai amoniac NH3
NH4NO3 + NaOH → NaNO3 + NH3 + H2O
Bài tập phản ứng Mg + HN03
Câu 1. Cho m gam Mg vào dung dịch chứa 0,12 mol FeCl3. Sau khi phản ứng xảy ra hoàn toàn thu được 3,36 gam chất rắn. Giá trị của m là
Giải:
Xét 2 trường hợp:
Trường hợp 1: Sau phản ứng Mg còn dư. Chỉ có phản ứng (1) khối lượng chất rắn thu được là Fe vào Mg dư
nFe= nFeCl3 = 0,12 mol => mFe = 0,12 . 56 = 6,72g > 3,36 (loại)
Trường hợp 2: Xảy ra 2 phản ứng (1) và (2) (khi Mg hết FeCl3 còn sẽ tác dụng tiếp với Fe)
Gọi số mol của Mg là: nMg = a mol
3Mg + 2FeCl3 → 3MgCl2 + 2Fe (1)
a ———> 2a/3 —————-> 2a/3
Fe + 2FeCl3 → 3FeCl2(2)
2a/3 – 0,06 –> 2 (2a/3 – 0,06)
nFe dư sau pư 2 = 3,36 : 56 = 0,06 mol => nFe (pư2)= (2a/3 – 0,06) mol
Theo phương trình phản ứng 1: 2nFeCl3= 2a/3 + 2(2a/3 – 0,06) = 0,12 mol
=> a = 0,12 mol
=> m = 0,12 . 24 = 2,88 g
Câu 2. Dung dịch nào dưới đây khi phản ứng hoàn toàn với dung dịch NaOH dư, thu được kết tủa trắng?
A. Ca(HCO3)2.
B. FeCl3.
C. AlCl3.
D. H2SO4.
Giải:
A đúng vì Ca(HCO3)2+ 2NaOH → CaCO3↓ trắng + Na2CO3 + 2H2O
B sai vì Fe(OH)3 kết tủa nâu đỏ: FeCl3+ 3NaOH → Fe(OH)3 ↓ + 3NaCl
C sai vì không thu được kết tủa: Al3+ + 4OH– dư → AlO2- + 2H2O
D sai vì không có kết tủa: H2SO4 + 2NaOH → Na2SO4 + H2O
Câu 3. Cho 1,38 g hổn hợp Al, Fe tác dụng với dung dịch hổn hợp H2SO4 đặc và HNO3 đặc, đun nóng thu được hổn hợp khí gồm 0,063 mol NO2 và 0,021 mol SO2. Nếu cho hổn hợp kim loại trên tác dụng với dung dịch HCl có dư thì số mol khí H2 sinh ra là bao nhiêu?
Giải:
Gọi số mol Al, Fe trong hỗn hợp là x, y
mhh = 27x + 56y = 1,38 (g) (1)
Al0 → Al+3 + 3e N+5 + 1e → N+4
x → 3x 0,063 ← 0,063
Fe0 → Fe+3 + 3e S+6 + 2e → S+4
y → 3y 0,042 ← 0,021
Áp dụng bảo toàn e: 3x + 3y = 0,063 + 0,042 = 0,105 (mol) (2)
Từ (1) và (2) → x = 0,02; y = 0,015
+) Hỗn hợp kim loại + HCl dư:
Al0 → Al+3 + 3e 2H+ + 2e → H2
0,02 → 0,06 0,09 → 0,045
Fe0 → Fe+2 + 2e
0,015 → 0,03
ne nhường= 0,06 + 0,03 = 0,09 => nH2 = 0,09/2 = 0,045 mol
Câu 4. Cho từng chất: Fe, FeO, Fe(OH)2, Fe(OH)3, Fe3O4, Fe2O3, Fe(NO3)2, Fe(NO3)3, FeSO4, Fe2(SO4)3, FeCO3 lần lượt phản ứng với HNO3 đặc, nóng. Số phản ứng thuộc loại phản ứng oxi hoá – khử là
Giải:
Các chất có phản ứng oxi hóa- khử là: Fe, FeO, Fe(OH)2, Fe3O4, Fe(NO3)2, FeSO4, FeCO3.
Fe + 6HNO3 → Fe(NO3)3+ 3NO2 ↑ + 3H2O
FeO + 4HNO3 → Fe(NO3)3 + NO2 + 2H2O
Fe(OH)2 + 4HNO3 → Fe(NO3)3 + NO2 + 3H2O
Fe3O4+ 10HNO3 → 3Fe(NO3)3 + NO2 + 5H2O
Fe(NO3)2 + 2HNO3→ Fe(NO3)3 + NO2 + H2O
FeSO4 + 4HNO3 → Fe(NO3)3+ H2SO4+ NO2 + H2O
FeCO3 + 4HNO3 → Fe(NO3)3 + CO2 + NO2 + 2H2O
Câu 5. Cho 0,896 lít CO2 hấp thụ hết vào 200 ml dung dịch chứa hỗn hợp NaOH 0,06M và Ba(OH)2 0,12M thu được m gam kết tủa. Giá trị m là:
Giải:
nCO2= 0,04 mol; nOH– = 0,06 mol
Có: 1 < nOH/nCO2 = 1,5<2
=>Tạo 2 muối là CO3(2-) (x mol) và HCO3(-) (y mol)
Ta có:
x + y = 0,042 (1)
x + y = 0,06 (2)
Giải hệ phương trình (1), (2)
<=> x = y = 0,02
=>nBaCO3= nCO3(2-)= 0,02 mol
=>mBaCO3= 3,94 g
Câu 6. Hỗn hợp X gồm 2 kim loại A và B thuộc phân nhóm chính nhóm II, ở 2 chu kỳ liên tiếp. Cho 2,56 gam X tan hoàn toàn trong dung dịch HCl dư thu được 2,24 lít khí H2 (đktc). Cô cạn dung dịch sau phản ứng, khối lượng muối khan thu được là
Giải:
Phương trình phản ứng: R + 2HCl → RCl2 + H2
Ta có nHCl = 2nH2 = 0,2 mol
mmuối = mkim loại + mCl– = 2,56 + 0,2. 35,5 = 9,66 gam.
Câu 7. Trong một cốc nước có chứa 0,03 mol Na+; 0,01 mol Ca2+; 0,01 mol Mg2+; 0,04 mol HCO3–; 0,01 mol Cl-; 0,01 mol SO42-. Nước trong cốc thuộc loại
Giải:
Đun nóng dung dịch:
2HCO3– → CO32- + CO2+ H2O
0,04 → 0,02 (mol)
Ta thấy Ca2+ và Mg2+ bị kết tủa hết:
Ca2+ + CO32- → CaCO3↓
0,01 → 0,01
Mg2+ + CO32- → MgCO3 ↓
0,01 → 0,01
Vậy nước cứng bị mất tính cứng khi đun nóng nên là nước cứng tạm thời.
Câu 8. Cho m gam Mg vào dung dịch chứa 9,75 gam FeCl3. Sau khi phản ứng xảy ra hoàn toàn thu được 1,68 gam chất rắn. Giá trị của m là :
Giải:
Mg + 2Fe3+ → Mg2+ + 2Fe2+ (1)
Mg + Fe2+ → Mg2+ + Fe (2)
Ta nhận thấy: 1,68 < 0,06.56 = 3,36
=> Sau phản ứng dung dịch muối chưa phản ứng hết
nFe sinh ra sau phản ứng = 1,68 /56 = 0,03 (mol)
(2) nFe = nMg = 0,03 (mol)
(1) nMg = 1/2nFeCl3 = 0,03 (mol)
=> nMg = 0,03 + 0,03 = 0,06 (mol)
=> mMg = 0,06 . 24 = 1,44 gam.
Sau khi đọc xong bài viết của chúng tôi bạn có thể biết được Mg + HN03 để vận dụng vào làm các bài tập từ cơ bản đến nâng cao nhanh chóng nhé