Cách xác định hóa trị của 1 nguyên tố và các dạng bài tập
Hóa trị là gì? Cách xác định hóa trị, quy tắc hóa trị? được chúng tôi soạn giúp bạn đọc có thêm tài liệu tham khảo về Bài 10 hóa 8 Hóa trị. Cũng như vận dụng quy tắc hóa trị linh hoạt vào giải các dạng bài tập liên đến hóa trị. Hy vọng giúp ích cho các bạn trong quá trình làm bài tập hóa trị. Mời các bạn tham khảo.
Tham khảo thêm:
- Phản ứng hóa học là gì? Khi nào phản ứng hóa học xảy ra và các dạng bài tập
- Dãy Điện Hóa là gì ? Cách đọc Dãy Điện Hõa kim loại dễ thuộc
- Bảng hóa trị của các nguyên tố và cách học thuộc bằng bài ca hóa trị
Nội Dung
Hóa trị là gì?
+) Hóa trị là của các nguyên tố xác định bằng số liên kết mà một nguyên tử của nguyên tố đó liên kết nên trong phân tử.
+) Hóa trị của nguyên tố ở hợp chất ion được gọi là điện hóa trị và nó có giá trị bằng với điện tích ion tạo thành từ nguyên tố ấy.
+) Hóa trị của nguyên tố ở hợp chất cộng hóa trị gọi là cộng hóa trị, và có giá trị bằng với số liên kết cộng hóa trị do nguyên tử của nguyên tố đó tạo được với nguyên tử của nguyên tố khác trong hợp chất.
Quy tắc hóa trị
Ta có quy tắc hóa trị như sau: Tích giữa chỉ số và hóa trị của nguyên tố này bằng tích giữa chỉ số và hóa trị của nguyên tố kia.
Theo quy tắc hóa trị thì:
x.a = y.b
Trong đó:
- x, y là các hóa trị của nguyên tố
- a, b là các chỉ số
- Nếu biết x, y và a (hoặc b) thì tính được b (hoặc a)
- Nếu biết a, b thì tìm được x, y để lập công thức hóa học
Chuyển thành tỉ lệ:
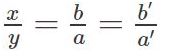
Lấy x = b (hoặc b’) và y = a (hoặc a’). Nếu a’, b’ là những số nguyên đơn giản hơn so với a, b.
Cách tính hóa trị một nguyên tố.
Hóa trị của một nguyên tố được xác định theo hóa trị của H chọn làm đơn vị và hóa trị của O là hai đơn vị.
Phương pháp:
- Gọi a là hóa trị của nguyên tố cần tìm.
- Áp dụng quy tắc về hóa trị để lập đẳng thức.
- Giải đẳng thức trên để tìm a
Chú ý:
- H và O đương nhiên đã biết hóa trị: H(I), O(II).
- Kết quả phải ghi số La Mã.
Các dạng bài tập xác định hóa trị thường gặp
Bài 1: Xác định hóa trị của S trong các hợp chất sau: H2S và SO2.
Giải:
+) Trong hợp chất H2S:
H có hóa trị I, gọi hóa trị của S là a ta có:
2.I = 1.a ⇒ a = II.
Vậy trong hợp chất H2S thì lưu huỳnh có hóa trị II.
+) Trong hợp chất SO2:
O có hóa trị II, gọi hóa trị của S là b, ta có:
1.b = 2.II ⇒ b = IV.
Vậy trong hợp chất SO2 thì lưu huỳnh có hóa trị IV.
Bài 2: Biết trong công thức hóa học K2SO4 thì K có hóa trị I. Hãy xác định hóa trị của nhóm (SO4).
Giải:
Gọi hóa trị của nhóm (SO4) là a.
Theo quy tắc hóa trị ta có: 2.I = 1.a ⇒ a = II.
Vậy nhóm (SO4) có hóa trị II.
Bài 3: Hãy chọn công thức hóa học phù hợp với hóa trị IV của nitơ trong số các công thức sau:
Giải:
Trong các công thức hóa học trên H có hóa trị I, O có hóa trị II.
– Xét NO:
Gọi N có hóa trị là a, ta có:
1.a = 1.II ⇒ a = II (loại).
– Xét N2O5:
Gọi N có hóa trị là a, ta có:
2.a = 5.II ⇒ a = V (loại).
– Xét NH3:
Gọi N có hóa trị là a, ta có:
1.a = 3.I ⇒ a = III (loại).
– Xét NO2:
Gọi N có hóa trị là a, ta có:
1.a = 2.II ⇒ a = IV (thỏa mãn).
Bài 4: Có các hợp chất: PH3, P2O3 trong đó P có hoá trị là
Giải:
+) Xét hợp chất PH3:
H có hóa trị I, gọi hóa trị của P là a.
Theo quy tắc hóa trị có: 1.a = 3.I ⇒ a = III.
+)Xét hợp chất P2O3:
O có hóa trị II, gọi hóa trị của P là b.
Theo quy tắc hóa trị có: 2.b = 3.II ⇒ b = III.
Vậy trong các hợp chất PH3 và P2O3 thì P có hóa trị III.
Bài 5: Biết trong công thức hóa học BaSO4 thì Ba có hóa trị II. Hóa trị của nhóm (SO4) là
Giải:
Đặt hóa trị của nhóm (SO4) là a.
Theo quy tắc hóa trị, ta có: 1.II = 1.a ⇒ a = II.
Vậy nhóm (SO4) có hóa trị II.
Bài 6: Một oxit có công thức Mn2Ox có phân tử khối là 222. Hoá trị của Mn trong oxit là
Giải:
Theo bài ra ta có: 2.55 + 16.x = 222.
Giải phương trình được x = 7.
Vậy oxit có công thức hóa học là Mn2O7.
Oxi có hóa trị II, gọi hóa trị của Mn là a. Theo quy tắc hóa trị có:
2.a = 7.II ⇒ a = VII.
Bài 7: Cho công thức hóa học H3PO4. Hóa trị của nhóm (PO4) là
Giải:
H có hóa trị I, gọi hóa trị của nhóm (PO4) là a.
Theo quy tắc hóa trị có: 3.I = 1.a ⇒ a = III.
Vậy nhóm (PO4) có hóa trị III.
Bài 8: Một oxit có công thức Al2Ox có phân tử khối là 102. Hóa trị của Al là
Giải:
Ta có: 27.2 + 16.x = 102.
Giải phương trình được x = 3. Vậy oxit là Al2O3.
Đặt a là hóa trị của Al. Ta có:
2.a = 3.II ⇒ a = III.
Bài 9: Xác định hóa trị của mỗi nguyên tố trong các trường hợp sau đây:
a) KH, H2S, CH4
b) FeO, Ag2O, NO2
Giải:
a) KH: Có H có hóa trị I, theo quy tắc hóa trị ta có: 1 x 1 = 1 x b => K hóa trị I.
H2S: có H có hóa trị I, theo quy tắc hóa trị, ta có: 2 x 1 = 1 x b => S hóa trị II.
CH4: có H có hóa trị I, theo quy tắc hóa trị, ta có: 1 x a = 4 x 1 => C hóa trị IV.
b) FeO: có O hóa trị II, theo quy tắc hóa trị, ta có: 1 x a = 2 x 1 => Fe hóa trị II
Ag2O: có O hóa trị II, theo quy tắc hóa trị, ta có 2 x a = 1 x 2 => Ag hóa trị I.
NO2: có O hóa trị II, theo quy tắc hóa trị, ta có: 1 x a = 2 x 2 => N hóa trị IV
Mong rằng những nội dung trên đây sẽ giúp bạn trả lời được những thắc mắc câu hỏi của mình. Hơn hết đó là có thể giải được những bài toán của mình