Tỉ khối của chất khí là gì? Công thức tỉ khối của chất khí và bài tập có lời giải chi tiết từ A- Z
Làm sao để biết được chất khí nào đó có những tính chất gì? Làm thế nào để chúng ta biết được chất khí đó nhẹ hay nặng hơn khí Hidro H2, khí Oxi O2 hay không khí. Vậy câu hỏi đặt ra là: Tỉ khối chất khí là gì? Tỉ khối của không khí? Công thức tính tỉ khối của chất khí như thế nào? Làm sao tính được tỉ khối so với không khí, với khí Oxi hay so với khí Hidro? Tất cả câu hỏi trên sẽ được giải đáp qua bài sau.
Tham khảo thêm:
- Liên kết cộng hóa trị là gì? Ý nghĩa liên kết cộng hóa trị và bài tập có lời giải chi tiết 100 %
- Phản ứng oxi hóa khử là gì? và các dạng bài tập từ cơ bản đến nâng cáo có lời giải
- Cách cân bằng phương trình hóa học oxi hóa khử và các dạng bài tập có lời giải chi tiết từ A- Z
Nội Dung
Tỉ khối của chất khí là gì?
Tỉ khối của chất khí là công thức giúp xác định phân tử khối của khí A so với khí B, để biết chất khí A nhẹ hay nặng hơn chất khí B bao nhiêu lần. Cách so sánh đó là khối lượng mol của hai chất khí đó với nhau MA và MB.
Công thức tính tỉ khối của chất khí
dA/B = MA/MB
Trong đó:
- dA/B là tỉ khối của khí A đối với khí B
- MA : khối lượng mol của khí A
- MB : khối lượng mol của khí B
+) Khi dA/B > 1 ⇒ khí A nặng hơn khí B
+) dA/B = 1 ⇒ khí A bằng khí B
+) dA/B < 1 ⇒ khí A nhẹ hơn khí B
Tỉ khối của khí A so với không khí
– Trong sinh học chúng ta đã biết không khí là hỗn hợp gồm nhiều khí, trong đó có hai khí chính là khí N2 chiếm khoảng 80% và khí O2 chiếm khoảng 20%. Do đó, khối lượng của “mol không khí” là khối lượng của 0,8 mol khí nitơ + khối lượng 0,2 mol khí oxi
=> Mkhông khí = 0,8.28 + 0,2.32 = 28,8 ≈ 29 gam
Công thức tỉ khối của khí A so với không khí:
dA/kk=MA/29
Trong đó:
- dA/kk : tỉ khối của khí A đối với không khí
- MA : khối lượng mol của khí A
- Mkk : khối lượng mol của không khí
Tỉ khối của hỗn hợp khí
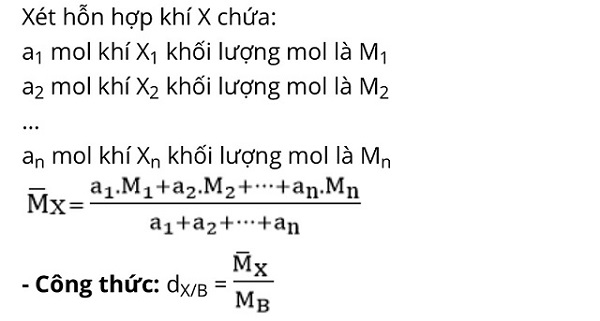
Tỉ khối của khí A nặng hay nhẹ hơn khí B
Để có thể biết khí A nặng hay nhẹ hơn khí B bao nhiêu lần rất đơn giản, ta chỉ cần so sánh khối lượng mol của khí A (ký hiệu là MA) với khối lượng mol của khí B (ký hiệu là MB).
Ta có công thức: dA/B = MA/ MB
Trong đó, dA/B là tỉ khối của khí A đối với khí B.
Ví dụ minh họa: Hãy xác định khí oxi nặng hay nhẹ hơn khí hiđro và nặng hay nhẹ hơn bao nhiêu lần?
Trả lời:
Dựa vào công thức xác định tỉ khối chất khí ta có:
Tỉ khối của O2/ H2 = Khối lượng mol của O2/ Khối lượng mol của H2 = 32/2 = 16.
Từ đó ta có thể kết luận rằng, không khí nặng hơn khí hiđro 16 lần.
Các dạng bài tập tỉ khối của chất khí thường gặp
Câu 1: Chất nào sau đây nặng hơn không khí?
A. SO2.
B. H2.
C. CH4.
D. N2.
Giải:
Không khí có M = 29 g/mol => chất nặng hơn không khí là chất có M > 29 g/mol
+) MSO2=32+16.2=64MSO2=32+16.2=64 > 29 => khí SO2 nặng hơn không khí
+) MH2=2.1=2MH2=2.1=2 < 29 => khí H2 nhẹ hơn không khí
+) MCH4=12+1.4=16MCH4=12+1.4=16 < 29 => khí CH4 nhẹ hơn không khí
+) MN2=2.14=28MN2=2.14=28 < 29 => khí N2 nhẹ hơn không khí
Đáp án cần chọn là: A
Câu 2: Dãy các chất khí đều nặng hơn không khí là:
A.SO2, Cl2, H2S
B. N2, CO2, H2
C. CH4, H2S, O2
D. Cl2, SO2, N2
Giải:
Dãy các chất khí đều nặng hơn không khí là: SO2, Cl2, H2S
B có N2( M=28) và H2(M=2) nhẹ hơn không khí
C có CH4 có M =16 nhẹ hơn không khí
D có N2 nhẹ hơn không khí
Đáp án cần chọn là: A
Câu 3: Tỉ khối của khí A đối với không khí là dA/KK< 1. Là khí nào?
Giải:
Có dA/KK< 1 => MA < Mkk = 29g/mol
MO2 = 32g/mol; MH2S = 34g/mol
MCO2 = 44g/mol; MN2 = 28g/mol
Câu 4: Một halogen X có tỉ khối hơi đối với canxi bằng 4. Xác định ký hiệu và tên gọi.
Giải:
Halogen có công thức phân tử là X2.
Áp dụng công thức tính tỉ khối:
X2 = 160 => 2X = 160 => X = 80X là brom, kí hiệu Br
Câu 5: Khí A có công thức dạng RO2. Biết dA/KK = 1,5862. Hãy xác định công thức của khí A.
Giải:
Tỉ khối của A so với không khí là 1,5862 => MA = 29 . dA/KK = 29.1,5862 = 46 g/mol
Khối lượng mol của khí A là
MRO2=MR+2.MO => MR = 46 – 2.16 = 14 gam
=> R là N
=> Công thức của A là NO2
Câu 6: Oxit có công thức hoá học RO2, trong đó mỗi nguyên tố chiếm 50% khối lượng. Khối lượng của R trong 1 mol oxit là:
Giải:
Ta có mỗi nguyên tố chiếm 50% khối lượng
=> %O = %R = 50%
Mặt khác %O = (MO : MRO2) . 100% = [32 : (MR + 32)] . 100% = 50%
=> MR = 32g/mol
1 mol RO2 có 1mol R => mR = 32 . 1 = 32g
Câu 7: Khí nào trong số các khí sau được thu bằng cách đẩy không khí úp bình?
Giải:
Vì khí hiđrô có MH2 = 2 , nhẹ hơn không khí nên có thể thu bằng phương pháp đẩy không khí úp bình
Khí CO2, Cl2 đều nặng hơn không khí nên không thu được bằng cách trên mà phải ngửa ống nghiệm.
Mong rằng những nội dung trên đây sẽ giúp bạn trả lời được những thắc mắc câu hỏi của mình. Hơn hết đó là có thể giải được những bài toán của mình