Lý thuyết Na + H2O → NaOH + H2 và bài tập có đáp án
Na + H2O → NaOH + H2 là phương trình phản ứng hóa học giữa kim loại Na cho tác dụng với nước, sau phản ứng có khí thoát ra. Dung dịch sau phản ứng làm quỳ tím hóa xanh. Hy vọng nội dung phương trình phản ứng Na tác dụng với nước sẽ giúp bạn đọc học tập cũng như làm bài tập tốt nhất. Mời các bạn tham khảo.
Tham khảo thêm:
Nội Dung
Phương trình Na tác dụng với H2O:
2Na + 2H2O → 2NaOH + H2
Điều kiện phản ứng giữa kim loại Na với H2O: Không có
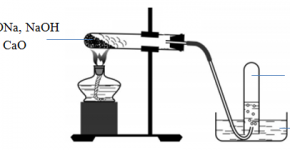
Cách thực hiện phản ứng kim loại Na với H2O: Cho mẫu natri vào cốc nước cất
Hiện tượng nhận biết phản ứng kim loại Na với H2O:
+) Natri phản ứng với nước, nóng chảy thành giọt tròn có màu trắng chuyển động nhanh trên mặt nước. Mẫu Na tan dần cho đến hết, có khí H2 bay ra, phản ứng toả nhiều nhiệt. Làm bay hơi nước của dung dịch tạo thành, sẽ được một chất rắn trắng, đó là Natri Hidroxit NaOH
Tính chất hóa học của kim loại kiềm
+) Các nguyên tử kim loại kiềm đều có năng lượng ion hóa I1 thấp và thế điện cực chuẩn E0 có giá trị rất âm. Vì vậy kim loại kiềm có tính khử rất mạnh.
Tác dụng với phi kim
+) Hầu hết các kim loại kiềm có thể khử được các phi kim.
Thí dụ: kim loại Na cháy trong môi trường khí oxi khô tạo ra natri peoxit Na2O2. Trong hợp chất peoxit, oxi có số oxi hóa -1:
Tác dụng với Oxi
+) Natri cháy trong khí oxi khô tạo ra natri peoxit Na2O2, trong không khí khô ở nhiệt độ thường tạo ra natri oxit Na2O
2Na + O2 → Na2O2
2Na + 1/2O2 → Na2O
b) Tác dụng với Clo
2K + Cl2 → 2KCl
+) Với halogen, lưu huỳnh:
Các kim loại kiềm bốc cháy trong khí clo khi có mặt hơi ẩm ở nhiệt độ cao. Với brom lỏng, K, Rb, Cs nổ mạnh, Li và Na chỉ tương tác trên bề mặt. Với iot, các kim loại kiềm chỉ tương tác mạnh khi đun nóng. Khi nghiền kim loại kiềm với bột lưu huỳnh sẽ gây phản ứng nổ.
* Với nitơ, cacbon, silic: Chỉ có Li có thể tương tác trực tiếp tạo Li3N, Li2C2, Li6Si2 khi đun nóng.
Kim loại kiềm tác dụng với axit
+) Các kim loại kiềm đều có thể khử dễ dàng ion H+ của dung dịch axit (HCl, H2SO4 loãng) thành khí H2 (phản ứng gây nổ nguy hiểm):
2Li + 2HCl → 2LiCl + H2↑
Dạng tổng quát:
2M + 2H+ → 2M+ + H2↑
Kim loại kiềm tác dụng với nước H2O
+) Kim loại kiềm khử được nước dễ dàng, giải phóng khí hiđro:
2Na + 2H2O → 2NaOH (dd) + H2↑
+) Dạng tổng quát:
2M + 2H2O → 2MOH (dd) + H2↑
+) Do vậy, các kim loại kiềm được bảo quản bằng cách ngâm chìm trong dầu hỏa.
Bài tập phản ứng NA + H2O
Câu 1. Có 2 lít dung dịch NaCl 0,5 M. Lượng kim loại và thể tích khí thu được (đktc) từ dung dịch trên là (hiệu suất điều chế bằng 90%)
Giải:
nNaCl= 1 (mol)
Phương trình hóa học
2NaCl → 2Na + Cl2
1 1 0.5
mNa= 1x 23 x 90/100 = 20.7 (g)
VCl2 = 0.5 x 22.4 x 90/100 = 10.08 (l)
Câu 2. Cho 1,84 gam hỗn hợp gồm Al và Zn tác dụng với một lượng vừa đủ dung dịch H2SO4 10% thu được 1,12 lít khí H2 (ở đktc). Khối lượng dung dịch thu được sau phản ứng là
Giải:
Ta có
nH2 = 1,12/22,4 = 0,05 mol → nH2SO4 = nH2= 0,05 mol
Khối lượng H2SO4 là: mH2SO4 = 0,05. 98 = 4,9 gam → mdd H2SO4 = (4,9.100)/10 = 49 gam
Khối lượng dung dịch sau phản ứng là:
mdd sau= mdd bđ+ mKL – mH2 = 49 + 1,84 – 0,05.2 = 50,74 gam
Câu 3. Đốt cháy hoàn toàn 6 gam hỗn hợp A gồm Al và Cu cần vừa đủ 2,912 lít hỗn hợp khí gồm O2 và Cl2 thu được 13,28 gam chất rắn. Phần trăm khối lượng của Al trong A là?
Giải:
Áp dụng định luật bảo toàn khối lượng
=> mO2 + mCl2 = mChất rắn – mKL = 13,28 – 6 = 7,28 gam
nO2+ nCl2 = 2,912:22,4 = 0,13 (mol)
Gọi số mol O2, Cl2 lần lượt là x, y
=> Ta có hệ phương trình:
x + y =0,13
32x + 71y = 7,28
=> x = 0,05; y = 0,08
Gọi số mol Al, Cu lần lượt là a, b
Áp dụng định luật bảo toàn electron:
=> Tổng lượng e nhường của kim loại bằng tổng lượng e nhận của phi kim (O2, Cl2)
=> 3a+ 2b = 4. nO2+ 2. nCl2
=> 3a + 2b = 4.0,05 + 2.0,08 = 0,36 (I)
Khối lượng của 2 kim loại bằng 3 gam
=> 27x + 64y = 6 (II)
Từ (I) và (II) => a = 0,08 ; b = 0,06
% Al = (0,08 . 27): 6 . 100% = 36%
Câu 4. Hỗn hợp X gồm Fe, FeO, Fe2O3. Cho một luồng khí CO đi qua ống sứ đựng m g hỗn hợp X nung nóng. Sau khi kết thúc thí nghiệm thu được 64 g chất rắn A và 11,2 lít khí B (đktc) có tỉ khối so với hiđro là 20,4. Giá trị của a là
Giải:
Gọi x, y lần lượt là số mol của: nCO = x (mol); nCO2 = y (mol)
Theo đề bài
nhh = 11,2/22,4 = 0,5 mol
Ta có hệ phương trình:
nhh= x + y = 0,5
mhh= 28x + 44y = 0,5.(20,8.2)
x = 0,1
y = 0,4
nCOpư = nCO2= 0,4 mol
Bảo toàn khối lượng: mCOpu + mX = mA+ mCO2
→ mX = 64 − 0.4 (44 − 28) = 70,4 gam
Câu 5. Cho thanh sắt Fe vào dung dịch X chứa 0,2 mol AgNO3 và 0,4 mol Cu(NO3)2. Khi thấy thanh kim loại tăng lên 17,6 gam thì dừng lại. Tính khối lượng kim loại bám vào thanh sắt
nAg+ = 0,1 mol;
nCu2+ = 0,2 mol
Nếu Ag+ phản ứng hết :
Fe + 2Ag+ → Fe2+ + 2Ag
0,1 ← 0,2 → 0,2
=> mtăng = 0,2.108 – 0,1.56 = 16 < 17,6
=> Ag+ phản ứng hết; Cu2+ phản ứng 1 phần
Fe + Cu2+ → Fe2+ + Cu
x → x → x
=> mtăng = 64x – 56x = 16x
=> tổng khối lượng tăng ở 2 phản ứng là:
mtăng = 16 + 16x = 17,6 => x = 0,1 mol
=> mkim loại bám vào = mAg + mCu= 17,2 gam
Sau khi đọc xong bài viết của chúng tôi bạn có thể biết được NA + H2O để vận dụng vào làm các bài tập từ cơ bản đến nâng cao nhanh chóng nhé