Liên kết ion là gì? Ý nghĩa liên kết ion và bài tập có lời giải chi tiết 100 %
Khi các phân tử thêm hoặc mất bớt electron trong quá trình phản ứng hóa học, tạo ra các phần tử mang điện được gọi là ion (liên kết tĩnh điện). Bản chất của liên kết ion là lực hút tĩnh điện giữa 2 ion mang điện tích trái dấu. Vậy liên kết ion là gì, được hình thành như thế nào? Bài viết sau đây sẽ giải đáp câu hỏi này một cách chi tiết nhất.
Tham khảo thêm:
- Tính chất hóa học của muối và các dạng bài tập liên quan chuẩn 100%
- Tính chất hóa học của kim loại và các dạng bài tập liên quan chuẩn 100%
- Tính chất hóa học của axit và các dạng bài tập liên quan chuẩn 100%
Nội Dung
Liên kết ion là gì?
Liên kết ion, hay liên kết điện tích, là một liên kết hóa học có bản chất là lực hút tĩnh điện giữa hai ion mang điện tích trái dấu.
Ví dụ về liên kết ion: Sự kết hợp giữa natri (Na+) và clorua (Cl–) tạo thành natri clorua (NaCl):
Na+ + Cl– → NaCl
Liên kết ion thường là liên kết giữa các nguyên tử nguyên tố phi kim với các nguyên tử nguyên tố kim loại.
Quy tắc bát tử
– Trong các nguyên tử khí hiếm, nguyên tử heli chỉ có 2 electron nên có 2 electron ở lớp thứ nhất cũng là lớp ngoài cùng, còn các nguyên tử khí hiếm khác để có 8 electron ở lớp ngoài cùng.
⇒ Như vậy, cấu hình với 8 electron ở lớp ngoài cùng (hoặc 2 electron đối với heli) là cấu hình electron vững bền.
– Theo quy tắc bát tử (8 electron) thì nguyên tử của các nguyên tố có khuynh hướng liên kết với các nguyên tử khác để đạt được cấu hình electron vững bền của các khí hiếm với 8 electron (hoặc 2 đối với heli) ở lớp ngoài cùng.
Liên kết ion
Sự hình thành ion
– Trong phản ứng hóa học, khi nguyên tử, phân tử thêm hoặc mất bớt electron nó sẽ tạo thành các phần tử mang điện được gọi là ion. Các ion trái dấu hút nhau bằng lực hút tĩnh điện tạo thành hợp chất chứa liên kết ion.
– Điều kiện hình thành liên kết ion:
+ Liên kết được hình thành giữa các nguyên tố có tính chất khác hẳn nhau (kim loại điển hình và phi kim điển hình).
+ Quy ước hiệu độ âm điện giữa hai nguyên tử liên kết ≥ 1,7 là liên kết ion (trừ một số trường hợp).
– Dấu hiệu cho thấy phân tử có liên kết ion:
+ Phân tử hợp chất được hình thành từ kim loại điển hình (kim loại nhóm IA, IIA) và phi kim điển hình (phi kim nhóm VIIA và Oxi).
– Đặc điểm của hợp chất ion: Các hợp chấy ion có nhiệt độ nóng chảy và nhiệt độ sôi cao, dẫn điện khi tan tròn nước hoặc nóng chảy.
– ion được chia thành cation và anion:
- Cation: ion dương
- Anion: ion âm
1. Sự tạo thành cation
– Ion mang điện tích dương gọi là ion dương hay cation.
– Nếu các nguyên tử nhường bớt electron khi tham gia phản ứng hóa học nó sẽ trở thành các phần tử mang điện tích dương hay còn gọi là cation.
2. Sự tạo thành anion
– Ion mang điện tích âm gọi là ion âm hay anion.
– Nếu các nguyên tử nhận thêm electron khi tham gia phản ứng hóa học nó sẽ trở thành các phần tử mang điện tích âm hay còn gọi là anion.
3. Ion đơn nguyên tử và ion âm đa nguyên tử
– Ion đơn nguyên tử là ion tạo nên từ 1 nguyên tử. Thí dụ cation Li+, Na+, Mg2+, Al3+và anion F –, Cl–, S2-, ……
– Ion đa nguyên tử là những nhóm nguyên tử mang điện tích dương hay âm . Thí dụ: cation amoni NH4+, anion hidroxit OH–, anion sunfat SO42–, …….
Sự tạo thành liên kết ion
Sự tạo thành liên kết ion của phân tử 2 nguyên tử
Xét sự hình thành liên kết ion trong phân tử natri clorua (NaCl)
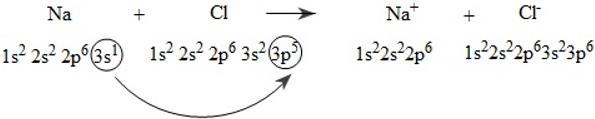
Hai ion được tạo thành mang điện tích ngược dấu hút nhau bằng lực hút tĩnh điện, tạo nên phân tử NaCl:
Na+ + Cl– → NaCl
Sự tạo thành liên kết ion trong phân tử nhiều nguyên tử
Xét sự hình thành liên kết ion trong phân tử CaCl2:
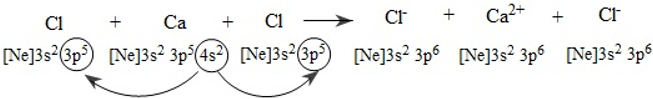
Các ion Ca2+ và Cl– tạo thành mang điện tích ngược dấu hút nhau bằng lực hút tĩnh điện, tạo nên phân tử CaCl2:
Ca2+ + 2Cl– → CaCl2
Vậy: Liên kết ion là liên kết được tạo thành do lực hút tĩnh điện giữa các ion mang điện tích trái dấu.Ngoài ra liên kết ion được hình thành giữa kim loại điển hình và phi kim điển hình.
Tinh thể mạng ion
Khái niệm về tinh thể
– Tinh thể được cấu tạo từ những nguyên tử, hoặc ion, hoặc phân tử.
Các hạt này được sắp xếp một cách đều đặn, tuần hoàn theo một trật tự nhất định trong không gian tạo thành mạng tinh thể.
– Các tinh thể thường có hình dạng không gian xác định.
Mạng tinh thể ion
Tinh thể NaCl được tạo bởi rất nhiều ion Na+ và Cl–, không có phân tử NaCl riêng biệt.
Được mô phỏng như hình dưới đây:
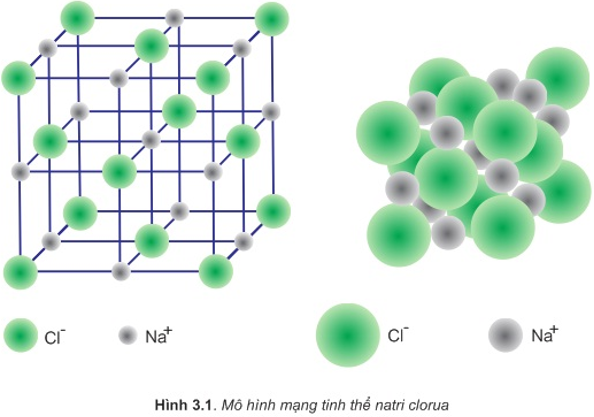
Tính chất chung của hợp chất ion
– Ở điều kiện thường, các hợp chất ion thường tồn tại ở dạng tinh thể, có tính biền vững, thường có nhiệt độ nóng chảy và nhiệt độ sôi khá cao.
– Các hợp chất ion chỉ tồn tại ở dạng phân tử riêng rẽ khi chúng ở trạng thái hơi.
– Các hợp chất ion thường tan nhiều trong nước. Khi nóng chảy và khi hòa tan trong nước, chúng dẫn điện, còn ở trạng thái rắn thì không dẫn điện.
Các dạng bài tập liên kết ion thường gặp
Bài 1: Viết cấu hình electron của Cl (Z = 17) và Ca (Z=20). Cho biết vị trí của chúng (chu kì, nhóm) trong bảng tuần hoàn. Liên kết giữa canxi và clo trong hợp chất CaCl2 thuộc loại liên kết gì? Vì sao? Viết sơ đồ hình thành liên kết đó.
Giải:
Cl (Z = 17) : 1s22s22p63s23p5
Ca (Z = 20) : 1s22s22p63s23p64s2
Clo nằm ở ô số 17, chu kỳ 3, nhóm VIIA.
Canxi nằm ở ô số 20, chu kỳ 4, nhóm IIA.
Liên kết trong hợp chất CaCl2 là liên kết ion vì Ca là kim loại điển hình, Cl là phi kim điển hình.
Sơ đồ hình thành liên kết:
2Cl + 21e → 2Cl–
Ca → Ca2+ + 2e
Các ion Ca2+và Cl–tạo thành mang điện tích trái dấu, chúng hút nhau bằng lực hút tĩnh điện, tạo thành hợp chất CaCl2:
Ca2+ + 2Cl– → CaCl2
Bài 2: Hai nguyên tố M và X tạo thành hợp chất có công thức là M2X. Cho biết:
– Tổng số proton trong hợp chất bằng 46.
– Trong hạt nhân của M có n – p = 1, trong hạt nhân của X có n’ = p’.
– Trong hợp chất M2X, nguyên tố X chiếm khối lượng.
1. Tìm số hạt proton trong nguyên tử M và X.
2. Dựa vào bảng tuần hoàn hãy cho biết tên các nguyên tố M, X.
3. Liên kết trong hợp chất M2X là liên kết gì? Tại sao? Viết sơ đồ hình thành liên kết trong hợp chất đó.
Giải:
1. Tổng số proton trong hợp chất M2X bằng 46 nên : 2p + p’ = 46. (1)
Trong hợp chất M2X, nguyên tố X chiếm khối lượng nên:
39p’ = 8(2p + 1). (2)
Từ (1), (2) ta tìm được: p = 19; p’ = 8.
2. M là kali (K) và X là oxi (O).
3. Liên kết trong hợp chất K2O là liên kết ion vì K là kim loại điển hình, O là phi kim điển hình.
Sơ đồ hình thành liên kết:
O + 2e → O2-
2K → 2K+ + 2.1e
Các ion K+và O2-tạo thành mang điện tích trái dấu, chúng hút nhau bằng lực hút tĩnh điện, tạo thành hợp chất K2O:
2K+ + O2- → K2O
Bài 3:
a, Viết cấu hình electron của các nguyên tử A, B biết rằng:
– Tổng số các loại hạt cơ bản trong nguyên tử A là 34. Số hạt mang điện nhiều hơn số hạt không mang điện là 10.
– Kí hiệu của nguyên tử B là B.
b, Liên kết trong hợp chất tạo thành từ A và B thuộc loại liên kết gì? Vì sao? Viết công thức của hợp chất tạo thành .
Giải:
a, Gọi tổng số hạt proton, nơtron, electron của nguyên tử A là P, N, E (trong đó P = E).
Ta có: P + N + E = 34 và P + E – N = 10.
Từ đây tìm được P = E = 11; N = 12.
Kí hiệu của nguyên tử B là B nên ZB = 9
Cấu hình electron của A, B:
A (Z = 11) : 1s22s22p63s1
B (Z = 9) : 1s22s22p5
b, Liên kết trong hợp chất giữa A và B là liên kết ion vì A là kim loại điển hình (nhóm IA), B là phi kim điển hình (nhóm VIIA).
Sơ đồ hình thành liên kết:
A → A+ + 1e
B + 1e → B–
Các ion A+và B- tạo thành mang điện tích trái dấu, chúng hút nhau bằng lực hút tĩnh điện, tạo thành hợp chất AB:
A+ + B– → AB.
Bài 4: a) Viết cấu hình electron của cation liti (Li+) và anion oxit (O2-).
b) Những điện tích ở ion Li+ và O2- do đâu mà có?
c) Nguyên tử khí hiếm nào có cấu hình electron giống Li+ và nguyên tử khí hiếm nào có cấu hình electron giống O2-.
d) Vì sao 1 nguyên tử oxi kết hợp được với 2 nguyên tử liti?
Giải:
a) Cấu hình electron của cation liti (Li+) là 1s2 và anion oxit (O2-) là 1s22s22p6.
b) Điện tích ở Li+ do mất 1e mà có, điện tích ở O2- do O nhận thêm 2e mà có.
c) Nguyên tử khí hiếm He có cấu hình electron giống Li+
Nguyên tử khí hiếm Ne có cấu hình electron giống O2-
d) Vì mỗi nguyên tử liti chỉ có thể nhường 1e, mà một nguyên tử oxi thu 2e.
2Li → 2Li+ + 2e;
O + 2e → O2-;
2Li+ + O2- → Li2O.
Bài 5 : So sánh số electron trong các cation sau: Na+, Mg2+, Al3+
Giải:
Các ion Na+, Mg2+, Al3+ đều có 10 electron.
Vì ZNa = 11 ⇒ Na có 11e ⇒ Na+ có 11 – 1 = 10e
ZMg = 12 ⇒ Mg có 12e ⇒ Mg2+ có 12 – 2 = 10e
ZAl = 13 ⇒ Al có 13e ⇒ Al3+ có 13 – 3 = 10e
Mong rằng những nội dung trên đây sẽ giúp bạn trả lời được những thắc mắc câu hỏi của mình. Hơn hết đó là có thể giải được những bài toán của mình