Ankin là gì? Tích chất, công thức tổng quát, cách điều chế ankin và bài tập ứng dụng
Trong chương trình Hoá học 11 các em sẽ được làm quen với các kiến thức liên quan đến nhóm akin. Vậy ankin là gì và có những tính chất nào? Cùng chúng tôi tìm hiểu rõ hơn những lý thuyết, tính chất và dãy đồng đẳng của ankin qua bài viết dưới đây.
Tham khảo thêm:
- Bảng Tính Tan Của Muối, muối nào tan trong nước và không tan
- Dãy Điện Hóa là gì ? Cách đọc Dãy Điện Hõa kim loại dễ thuộc
- Bảng hóa trị của các nguyên tố và cách học thuộc bằng bài ca hóa trị
Nội Dung
Ankin là gì?
Ankin là hidrocacbon không no, trong phân tử có liên kết ba C≡C có công thức phân tử dạng tổng quát là: CnH2n-2 (n≥2).
Tên gọi của ankin
Trong dãy Ankin thì axetilen có công thức đơn giản nhất C2H2: CH≡CH Tên gọi của Ankin (danh pháp)
• Tên thường: Tên gốc hiđrocacbon gắn với C mang liên kết ba + axetilen Ví dụ: CH≡CH: axetilen ; CH≡C-CH2-CH3: etylaxetilen ; CH3-C≡C-CH3: đimetylaxetilen ;
• Tên thay thế: Số chỉ vị trí mạch nhánh + tên nhánh + tên mạch chính + số chỉ vị trí nối ba + in Ví dụ: CH≡CH: etin ; CH≡C-CH3: propin ; CH≡C-CH2-CH3: but-1-in
Đồng đẳng, đồng phân, danh pháp
Đồng đẳng, cấu tạo
Công thức chung: CnH2n-2 (n ≥ 2).
Công thức đơn giản nhất là axetilen (CH≡CH).
+) Trong phân tử có 1 liên kết ba: gồm 1 liên kết σ và 2 liên kết π. Nguyên tử cacbon ở liên kết ba tham gia 2 liên kết σ nhờ 2 obitan lai hóa sp, còn 2 liên kết π nhờ 2 obitan p không lai hóa.
+) Đặc biệt phân tử CH≡CH có cấu trúc đường thẳng.
+) Trong phân tử C2H2 có 2 liên kết π làm độ dài liên kết C≡C giảm so với liên kết C=C và C-C. Các nguyên tử cacbon không thể quay tự do quanh liên kết 3.
Danh pháp, đồng phân
1. Danh pháp
– Tên gọi gồm: tên mạch cacbon có đuôi in
- C2H2: Etin
- C3H4: Propin
- C4H6: Buten
- C5H8: Pentin
- C6H10: Hexin
- C7H16: Hepten
- C8H14: Octin
- C9H16: Nonin
- C10H22: Đecen
+) Mạch chính là mạch cacbon có nối ba với số thứ tự của cacbon ở nối ba nhỏ nhất.
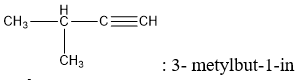
Đồng phân
Hiện tượng đồng phân do: Mạch cacbon khác nhau, vị trí nối ba khác nhau. Ngoài ra còn có đồng phân dạng: ankadien và hiđrocacbon vòng.
+)Từ C4 trở đi mới có đồng phân.
Ví dụ: C5H8 có 3 đồng phân.
CH≡C–CH2–CH2–CH3; CH3–C≡C–CH2–CH3
CH≡C–CH(CH3)–CH3
Tính chất vật lý của ankin
+) Nhiệt độ nóng chảy nhiệt độ sôi tăng dần khi tăng số nguyên tử cacbon trong phân tử: 3 chất đầu là khí, các chất có n từ 5 → 16 là chất lỏng, khi n ≥ 17 là chất rắn.
+) Đều ít tan trong nước, tan được trong một số dung môi hữu cơ (rượu, ete, …).
Tính chất hóa học của ankin
Phản ứng cộng hợp
+) Phản ứng cộng hiđrô
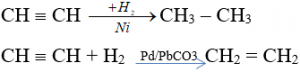
+) Phản ứng cộng brom, clo
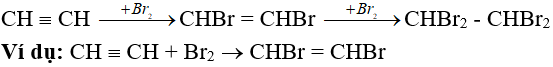
+) Phản ứng cộng HX (X là OH; Cl; Br; CH3COO, …)
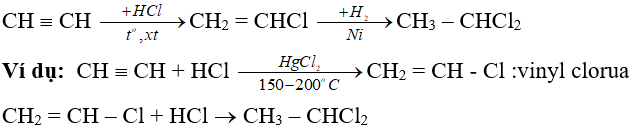
+) Phản ứng cộng của ankin với HX cũng tuân theo quy tắc Maccopnhicop.
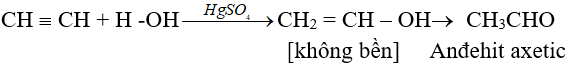
+) Phản ứng đimehoá, trimehoá
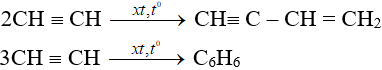
Phản ứng thế bằng ion kim loại
+) Phản ứng của ank-1-in
CH≡CH + AgNO3 + NH3 → CAg≡CAg↓ (Bạc Axetilen) + 2NH4NO3
Nhận xét: Phản ứng này dùng để phân biệt ank-1-in với anken và ankan.
Phản ứng oxi hoá ankin
+) Phản ứng oxi hóa hoàn toàn
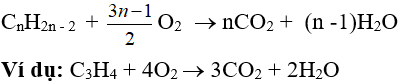
Phản ứng oxi hoá không hoàn toàn: tương tự anken và ankađien, ankin cũng có khả năng làm mất màu dung dịch KMnO4.
Điều chế và ứng dụng của ankin
Điều chế ankin
+) Điều chế axetilen
Tổng hợp trực tiếp:
![]()
Từ metan::
![]()
Từ canxi cacbua:
![]()
Tách H2 từ etan:
![]()
+) Điều chế các ankin khác:
Tách HX khỏi dẫn xuất đihalogen:
CH2Br-CH2Br + 2KOH → CH≡CH + 2KBr + 2H2O
Phản ứng giữa axetilua với dẫn xuất halogen:
CH3I + AgC ≡ CAg + CH3I → CH3 – C ≡ C – CH3 + 2AgI
Ứng dụng của ankin
+) Axetilen dùng trong đèn xì axetilen – oxi để hàn và cắt kim loại do axetilen cháy tạo ra ngọn lửa ở khoảng 3000oC.
+) Axetien và các akin khác còn được dùng làm nguyên liệu để tổng hợp các hóa chất khác như vinyl clorua, vinyl axetat, vinyl axetilen, …
Một số bài tập vận dụng về ankin
Bài 1 a) Viết công thức cấu tạo và gọi tên các ankin có công thức C4H6 và C5H8.
b) Viết công thức cấu tạo của các ankin có tên sau: pent-2-in ; 3-metylpent-1-in; 2,5- đimetylhex-3-in
Giải:
a) Công thức cấu tạo có thể có của ankin có công thức phân tử C4H6 là:
CH≡CH-CH2-CH3: But-1-in
CH3-C≡C-CH3: But-2-in
– Công thức cấu tạo có thể có của ankin có công thức phân tử C5H8 là:
CH≡CH-CH2-CH2-CH3: Pent-1-in
CH3-C≡C-CH2-CH3: Pent-2-in
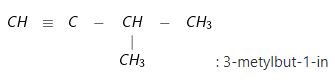
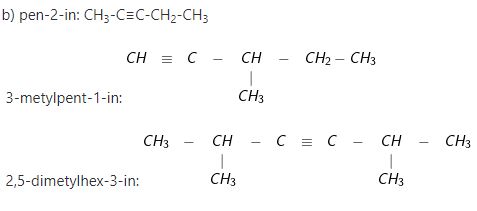
Bài 2 : Viết phương trình hóa học của phản ứng giữa propin và các chất sau:
a) hidro có xúc tác Pd/PbCO3
b) dung dịch brom (dư)
c) dung dịch bạc nitrat trong amoniac
Giải:
a) CH≡C-CH3 + H2 → CH2=CH-CH3
b) CH≡C-CH3 + 2Br2 (dư) → CHBr2-CBr2-CH3
c) CH≡C-CH3 + AgNO3 + NH3 → AgC≡C-CH3 + NH4NO3
Bài 3: Trình bày phương pháp hóa học:
a) Phân biệt axetilen với etilen
b) Phân biệt ba bình không dán nhãn chứa mỗi khí không màu sau: metan, etilen, axetilen
Giải:
a) Cho tác dụng với dung dịch AgNO3 trong NH3 dư, chất nào tạo kết tủa thì đó là axetilen, chất nào không tạo kết tủa thì là etilen.
– Phương trình phản ứng:
CH ≡CH + 2AgNO3 + 2NH3 → AgC≡CAg↓ +2NH4NO3
b) Lấy từ 3 bình các mẫu nhỏ để phân biệt.
– Lần lượt dẫn các mẫu khí qua dung dịch AgNO3/NH3, mẫu nào làm dung dịch xuất hiện kết tủa thì đó là axetilen
CH ≡CH + 2AgNO3 + 2NH3 → AgC≡CAg↓ +2NH4NO3
– Lần lượt dẫn 2 mẫu khí còn lại qua dung dịch brom, mẫu khí nào làm nhạt màu nước brom là etilen.
CH2=CH2 + Br2 → BrCH2=CH2Br
– Mẫu còn lại là metan.
Bài 4: Cho các chất sau: metan,etilen, but-2-in và axetilen. Kết luận nào sau đây là đúng?
A. Cả 4 chất đều có khả năng làm mất màu dung dịch brom
B. Có 2 chất tạo kết tủa với dung dịch bạc nitrat trong amoniac
C. Có ba chất có khả năng làm mất màu dung dịch Brom
D. Không có chất nào làm nhạt màu dung dịch kali pemangalat
Giải:
– Đáp án: C. Có ba chất có khả năng làm mất màu dung dịch Brom (do có liên kết π)
– Phương trình hóa học:
CH2=CH2 +Br2 → CH2Br-CH2Br
CH3-C≡C-CH3 + 2Br2→CH3-CBr2-CBr2 –CH3
CH≡CH + 2Br2→CHBr2 -CHBr2
Bài 5 : Dẫn 3,36 lít khí hỗn hợp A gồm propin và eilen đi vào một lượng dư dung dịch AgNO3 trong NH3 thấy còn 0,840 lít khí thoát ra và có m gam kết tủa. Các thể tích khí đo ở đktc.
a) Tính phần trăm thể tích etilen trong A
b) Tính m
Giải:
a) Khi dẫn hỗn hợp A đi qua dung dịch AgNO3/NH3 (dư) thì propin sẽ tác dụng hết với AgNO3/NH3, etilen không tác dụng.
⇒ 0,840 lít khí thoát ra là etilen: %VC2H4 = 0,84/3,36 x 100% = 25%.
b) Thể tích proprin là: 3,36 – 0,84 = 2,52 (lít).
⇒ nC3H4 (CH≡C-CH3) = 2,52/22,4 = 0,1125(mol).
CH≡C-CH3 + AgNO3 + NH3 → CAg≡C-CH3↓ + NH4NO3
0,1125 mol 0,1125 mol
– Từ PTPƯ ⇒ nCAg≡C-CH3↓ = nC3H4 = 0,1125
mCAg≡C-CH3↓ = n.MCAg≡C-CH3↓ = 0,1125. 147 = 16,5375(g).
Mong rằng những nội dung trên đây sẽ giúp bạn trả lời được những thắc mắc câu hỏi của mình. Hơn hết đó là có thể giải được những bài toán của mình