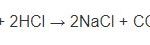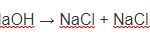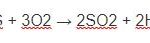Lý thuyết NaHCO3 + HCl → NaCl + CO2 + H2O và bài tập có đáp án
NaHCO3 + HCl → NaCl + CO2 + H2O là phương trình phản ứng hóa học khi cho NaHCO3 tác dụng với dung dịch axit HCl, tài liệu sẽ giúp các bạn học sinh viết và cân bằng chính xác.
Tham khảo thêm:
- CH3CHO + AgNO3 + NH3+ H2O → CH3COONH4 + NH4NO3 + Ag
- 2FeCl2 + Cl2 → 2FeCl3: Lý thuyết và bài tập có đáp án
- S + H2SO4 → SO2 + H2O: Lý thuyết và bài tập có đáp án
Nội Dung
Phương trình NaHCO3 ra CO2:
NaHCO3 + HCl → NaCl + CO2+ H2O
Điều kiện phản ứng NaHCO3 ra NaCl: Không có
Cách thực hiện phản ứng HCl tác dụng với NaHCO3: Cho HCl vào ống nghiệm đựng dung dịch NaHCO3
Hiện tượng nhận biết phản ứng NaHCO3 ra NaCl:
Cho HCl vào ống nghiệm đựng dung dịch NaHCO3 sau phản ứng Có bọt khí thoát ra là CO2. Muối cacbonat tác dụng với dung dịch axit mạnh hơn axit cacbonic tạo thành muối mới và giải phóng CO2
Tính chất hóa học của NaHCO3
Natri hiđrocacbonat là gì?
+) Natri hiđrocacbonat là một chất ở dạng bột mịn, trắng, dễ hút ẩm nhưng lại ít tan trong nước. khi có sự hiện diện của ion H+ thì khí CO2 sẽ được tạo ra.
+) Natri hiđrocacbonat có tên phổ biến trong hoá học là natri bicacbonat ( là tên của muối công thức hoá học NaHCO3). Ngoài ra, vì được sử dụng rất phổ biến trong thực phẩm nên Natri hiđrocacbonat còn có nhiều tên gọi khác như: bread soda, cooking soda, baking soda,…
Nhiệt phân tạo thành muối và giải phóng CO2
Tiến hành nhiệt phân hóa chất soda baking sẽ tạo ra muối mới và giải phóng khí CO2. Phương trình phản ứng như sau:
2NaHCO3 → Na2CO3 + CO2↑ + H2O
Thủy phân tạo thành môi trường Bazơ yếu
Phản ứng với nước, NaHCO3 sẽ bị thủy phân tạo ra môi trường bazơ yếu.
NaHCO3 + H2O → NaOH + H2CO3
Tác dụng với axit mạnh tạo thành muối và nước
Khi được sử dụng, hoặc tiếp xúc với các axit mạnh, NaHCO3 sẽ tạo thành dung dịch muối và nước, đồng thời giải phóng khí CO2.
Tác dụng với Axit Sunfuric
2NaHCO3 + H2SO4 → Na2SO4 + 2H2O + 2CO2
Tác dụng với axit Clohiric
NaHCO3 + HCl → NaCl + H2O + CO2
+) Tác dụng với bazơ tạo thành muối mới và bazơ mới
Khi được tác dụng với bazơ, NaHCO3 sẽ tạo ra muối mới và bazơ mới. Phương trình phản ứng như sau:
+) Tác dụng với Ca(OH)2
NaHCO3 + Ca(OH)2 → CaCO3 + NaOH + H2O.
+) Một trường hợp khác có thể tạo thành 2 muối mới với phương trình phản ứng:
2NaHCO3 + Ca(OH)2 → CaCO3 + Na2CO3 + 2H2O.
+) Tác dụng với NaOH:
NaHCO3 + NaOH → H2O + Na2CO3
+) Tác dụng với Ba(OH)2
2NaHCO3+ Ba(OH)2 → Na2CO3 + Ba2CO3 + 2H2O
Bài tập phản ứng NaHCO+HCl
Câu 1. Khi nung 60 gam hỗn hợp CaCO3 và MgCO3 thì khối lượng chất rắn thu được sau phản ứng chỉ bằng một nửa khối lượng ban đầu. Thành phần % theo khối lượng các chất ban đầu là
Giải:
Gọi số x, y lần lượt là số mol CaCO3 và MgCO3 trong hỗn hợp
Ta có: 100x + 84y = 60 (1)
Phương trình hóa học:
CaCO3 → CaO + CO2
x → x → x
MgCO3→ MgO + CO2
y → y → y
Áp dụng định luật bảo toàn khối lượng:
mhh trước = mcr sau + mkhí→ mkhí= 60 – 30 = 30 gam.
→ nkhí = 30/44 → x + y = 30/44.
Giải hệ có x = 0,17 và y = 0,452
%mCaCO3 = (0,17.100)/60 .100 = 28,33%
%mMgCO3 = 100% – 28,33% = 71,67%
Câu 2. Dung dịch Ca(OH)2 phản ứng với dãy chất nào sau đây?
A. BaCl2, K2CO3, Al.
B. CO2, K2CO3, Ca(HCO3)2.
C. NaCl, K2CO3, Ca(HCO3)2.
D. NaHCO3, NH4NO3, MgCO3.
Giải:
CO2 + Ca(OH)2 → CaCO3 ↓ + H2O
K2CO3 + Ca(OH)2→ CaCO3 ↓ + 2NaOH.
Ca(HCO3)2 + Ca(OH)2 → 2CaCO3↓ + 2H2O
Câu 3. Hỗn hợp X chứa K2O, NH4Cl, KHCO3 và BaCl2 với số mol các chất bằng nhau. Cho hỗn hợp X vào nước dư và đun nóng. Các chất tan trong dung dịch thu được là:
Giải:
Phản ứng xảy ra khi hỗn hợp tác dụng với nước:
K2O + H2O → 2KOH
Các phản ứng xảy ra tiếp theo:
NH4Cl + KOH → NH3 + H2O + KCl
KHCO3 + KOH → K2CO3 + H2O
K2CO3 + BaCl2 → BaCO3 + KCl
Vậy sau phản ứng dung dịch còn lại KCl
Câu 4. Nhỏ từ từ từng giọt đến hết 60 ml dung dịch HCl 1M vào 200 ml dung dịch chứa Na2CO3 0,2M và NaHCO3 0,2M, sau phản ứng thu được số mol CO2 là
Giải:
Nhỏ từ từ HCl vào dung dịch thứ tự phản ứng:
H+ + CO32- → HCO3– (1)
H+ + HCO3– → CO2 + H2O (2)
nH+ = 0,06 mol
nCO32- = 0,04 mol < nH+
nH+ (2) = nCO2 = 0,06 – 0,04 = 0,02 mol
Câu 5. Nhỏ từ từ từng giọt đến hết 30 ml dung dịch HCl 1M vào 100 ml dung dịch chứa Na2CO3 0,2M và NaHCO3 0,2M, sau phản ứng thu được số mol CO2 là
Giải:
Nhỏ từ từ HCl vào dung dịch thứ tự phản ứng:
H+ + CO32- → HCO3– (1)
H+ + HCO3– → CO2 + H2O (2)
nH+ = 0,03 mol
nCO32- = 0,02 mol < nH+
nH+ (2) = nCO2 = 0,03 – 0,02 = 0,01 mol
Câu 6. Cho 3,36 gam hỗn hợp gồm K và một kim loại kiềm A vào nước thấy thoát ra 1,792 lít H2. Thành phần phần trăm về khối lượng của A là
Giải:
Gọi công thức tổng quát chung của 2 kim loại kiềm là M
Phương trình phản ứng xảy ra
M + H2O → MOH + 1/2 H2
nM = 2nH2 = 1,792/22,4 = 0,16 mol => M = 3,36/0,16 = 21
Ta có Li (7) < M = 21 < K (39)
Gọi x, y lần lượt là số mol của K và Li
Ta có:
39 x + 7y = 3,36 => x = 0,07 mol, y = 0,09 mol
x + y = 0,16
%mLi = 0,09.7/3,36.100% = 18,75%
Câu 7. Khi cho kim loại Na vào dung dịch CuSO4 thì sẽ xảy ra hiện tượng nào sau đây?
Giải:
Khi cho kim loại Na vào dung dịch CuSO4 thì sẽ xảy ra hiện tượng:
Ban đầu, Na sẽ tác dụng với nước trước tạo NaOH và sủi bọt khí, sau đó có kết tủa xanh và không tan
Phương trình hóa học
2Na + 2H2O → 2NaOH + H2
2NaOH + CuSO4 → Na2SO4 + Cu(OH)2
Sau khi đọc xong bài viết của chúng tôi bạn có thể biết được NaHCO+HCl để vận dụng vào làm các bài tập từ cơ bản đến nâng cao nhanh chóng nhé