Ankan là gì? Công thức tổng quát, tính chất và cách điều chế ankan kèm theo bài tập
Trong chương trình Hoá học 11 các em sẽ được làm quen với các kiến thức liên quan đến nhóm akan. Vậy ankan là gì và có những tính chất nào? Cùng chúng tôi tìm hiểu rõ hơn những lý thuyết, tính chất và dãy đồng đẳng của ankan qua bài viết dưới đây.
Tham khảo thêm:
- Clorua vôi là gì ? Công thức, Tính Chất, Tác Hại của Ca(ClO)2
- Hiệu Suất là gì ? Công thức tính hiệu suất phản ứng hóa học
- Công thức tính nồng độ mol, số mol và C nồng độ phần trăm
Nội Dung
Ankan là gì
Ankan là những hydrocacbon no, mạch hở, trong phân tử chỉ có liên kết đơn C-C hoặc C-H. Công thức tổng quát của ankan: CnH2n+2 (n ≥ 1) Ankan đơn giản nhất là metan (CH4).
Công thức tổng quát chung cho ankan là CnH2n+2 (n ≥ 1)
Công thức đơn giản nhất là metan (CH4).
Tên gọi của ankan
Tên gọi của Ankan (danh pháp)
– Cách gọi tên Ankan mạch cacbon thẳng: Tên mạch cacbon + an
CH4: Metan ; C2H6: Etan ; C3H8: Propan ; C4H10: Butan ; C5H12: Pentan
C6H14: Hexan ; C7H16: Heptan ; C8H18: Octan ; C9H20: Nonan ; C10H22: Đecan * Cách nhớ gợi ý: Mẹ (Metan) Em (Etan) Phải (Propan) Bón (Butan) Phân (Pentan) Hóa (Hexan) Học (Heptan) Ở (Octan) Ngoài (Nonan) Đồng (Đecan).
– Cách gọi tên Ankan khi mạch cacbon có nhánh:
+ Chọn mạch chính : là mạch dài nhất có nhiều nhóm thế nhất.
+ Đánh số vị trí cacbon trong mạch chính bắt đầu từ phía gần nhánh hơn.
+ Gọi tên: Vị trí mạch nhánh + tên nhánh + tên mạch chính (tên ankan tương ứng với số nguyên tử cacbon trong mạch chính).
Công thức hóa học, đồng đẳng, đồng phân của ankan.
Đồng phân của ankan
+) Đồng phân mạch cacbon: Ankan chỉ có đồng phân mạch C khi có từ 4C trở lên.
Ví dụ: Các đồng phân của C5H12.
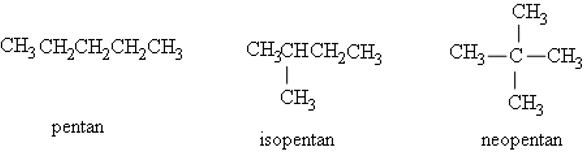
+) Bậc của cacbon: Bậc của 1 nguyên tử cacbon ở phân tử ankan bằng số nguyên tử C liên kết trực tiếp với nó.
Ví dụ;
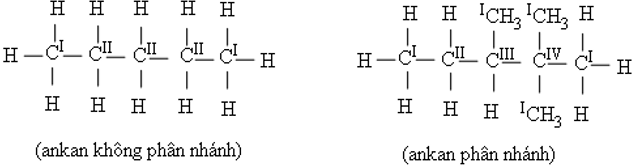
+) Ankan không phân nhánh là ankan chỉ chứa nguyên tử C bậc I hoặc bậc II.
+) Ankan phân nhánh là ankan có chứa C bậc III hoặc C bậc IV.
Đồng đẳng của ankan
CH4 và các chất có công thức phân tử như C2H6, C3H8, C4H10, C5H12,… là dãy đồng đẳng ankan với công thức tổng quát CnH2n+2 (n ≥ 1).
Trong phân tử ankan (trừ C2H6), các nguyên tử cacbon trong không cùng nằm trên một đường thẳng
Danh pháp của ankan
Tên gọi gồm: tên mạch cacbon có đuôi an.
- CH4: Metan
- C2H6: Etan
- C3H8: Propan
- C4H10: Butan
- C5H12: Pentan
- C6H14: Hexan
- C7H16: Heptan
- C8H18: Octan
- C9H20: Nonan
- C10H22: Đecan
Phân tử có mạch nhánh thì gọi theo quy tắc sau:
- Chọn mạch chính: là mạch dài nhất có nhiều nhóm thế nhất.
- Đánh số vị trí cacbon trong mạch chính bắt đầu từ phía gần nhánh hơn.
- Gọi tên: Vị trí mạch nhánh + tên nhánh + tên mạch chính (tên ankan tương ứng với số nguyên tử cacbon trong mạch chính).
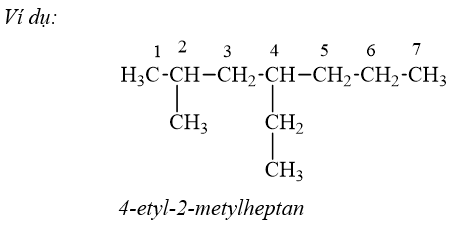
Lưu ý: Tên thường: Nếu chỉ có một nhánh duy nhất CH3 ở nguyên tử C số 2 thì thêm tiền tố iso.
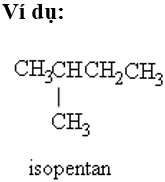
+) Nếu có 2 nhánh CH3 ở C số 2 thì thêm tiền tố neo.
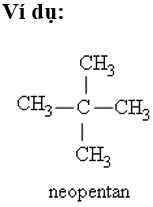
Cấu trúc phân tử ankan
Sự hình thành liên kết trong phân tử ankan:
- Các nguyên tử C ở trạng thái lai hóa sp3.
- Mỗi nguyên tử C nằm ở tâm mà 4 đỉnh là các nguyên tử H hoặc C.
- Liên kết C-C, C-H đều là liên kết σ.
- Các góc liên kết xấp xỉ 109,5o.
Cấu trúc không gian của ankan:
+)Mô hình phân tử
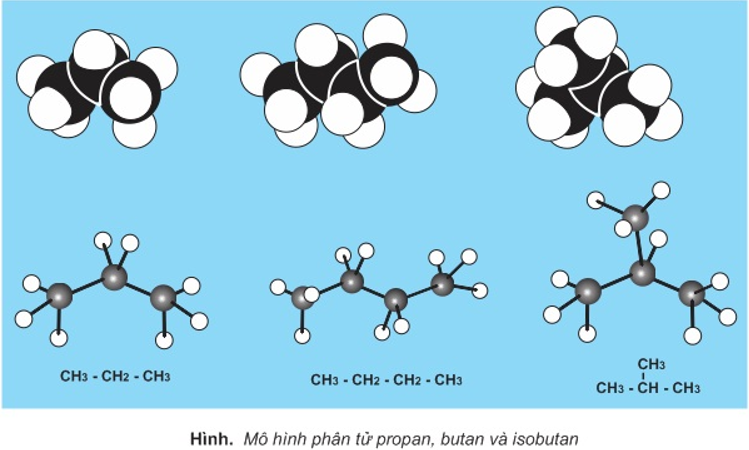
+) Cấu dạng
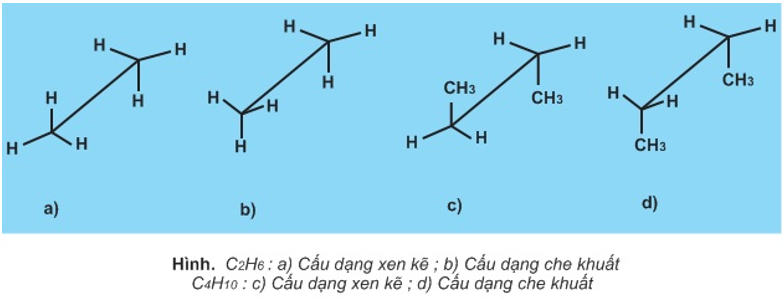
+) Các liên kết đơn C-C có thể quay tự do quanh trục liên kết tạo ra vô số dạng khác nhau về vị trí tương đối trong không gian gọi là các cấu dạng.
+) Cấu dạng xen kẽ bền hơn cấu dạng che khuất.
+) Các cấu dạng luôn chuyển đổi cho nhau.
Tính chất vật lý của ankan
+) Ở điều kiện thường, các ankan từ C1 đến C4 ở trạng thái khí, từ C5 đến khoảng C18 ở trạng thái lỏng, từ khoảng C18 trở đi ở trạng thái rắn.
+) Nhiệt độ nóng chảy, nhiệt độ sôi tăng dần khi tăng số nguyên tử cacbon trong phân tử: 4 chất đầu là chất khí, các chất có n từ 5 đến 19 là chất lỏng, khi n ≥ 20 là chất rắn.
+) Đều không tan trong nước nhưng dễ tan trong các dung môi hữu cơ.
+) Ankan đều là những chất không màu.
+) Các ankan nhẹ nhất như metan, etan, propan là những khí không mùi. Ankan từ C5 − C10 có mùi xăng, từ C10 − C16 có mùi dầu hỏa. Các ankan rắn rất ít bay hơi nên hầu như không mùi.
Tính chất hóa học của ankan
Phản ứng thế bởi halogen
+) Thế clo và brom: Xảy ra dưới tác dụng của askt hoặc nhiệt độ và tạo thành một hỗn hợp sản phẩm.
+) Phản ứng thế H bằng halogen thuộc loại phản ứng halogen hóa, sản phẩm hữu cơ có chứa halogen gọi là dẫn xuất halogen.
+) Clo thế H ở cacbon bậc khác nhau; Brom hầu như chỉ thế H ở cacbon bậc cao. Flo phản ứng mãnh liệt nên phân hủy ankan thành C và HF. Iot quá yếu nên không phản ứng với ankan.
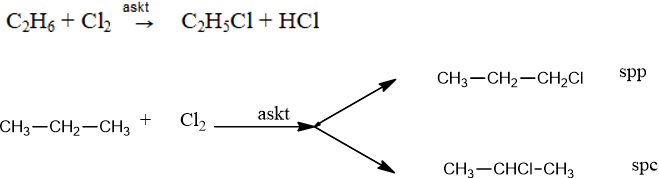
+) Những ankan có phân tử lớn tham gia phản ứng thế êm dịu hơn và ưu tiên thế những nguyên tử H của nguyên tử C bậc cao cho sản phẩm chính.
Phản ứng tách của ankan
+) Phản ứng tách hiđro: ở 400 – 900ºC, xúc tác Cr2O3 + Al2O3.
CH3–CH2-CH3 → CH3-CH=CH2 + H2
+) Phản ứng phân cắt mạch cacbon:
C5H12 → C2H6 + C3H6
Nhận xét: Dưới tác dụng của nhiệt và xúc tác (Cr2O3, Fe, Pt, …) các ankan không những bị tách hiđro tạo thành hiđrocacbon không no mà còn bị gãy các liên kết C−C tạo ra các phân tử nhỏ hơn.
Phản ứng phân hủy của Ankan
– Ankan bị phân hủy bởi nhiệt:
![]()
– Phản ứng phân hủy bởi halogen (Cl2 hoặc F2):
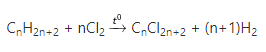
+ Ankan thẳng CnH2n+2 khi crăcking có thể xảy ra theo (n – 2) hướng khác nhau tạo ra 2(n-2) sản phẩm.
+ Nếu hiệu suất phản ứng crăcking là 100% và không có quá trình cracking thứ cấp thì tổng số mol sản phẩm tăng gấp đôi so với các chất tham gia nên KLPTTB giảm đi một nửa.
+ Số mol ankan sau phản ứng luôn bằng số mol ankan ban đầu dù quá trình cracking có nhiều giai đoạn
![]()
Phản ứng oxi hoá của ankan
Phản ứng đốt cháy ankan tạo CO2, H2O và tỏa nhiều nhiệt:
CnH2n+2 + O2 → nCO2 + (n + 1)H2O (1)
Nhận xét:
- Đốt ankan thu nCO2 < nH2O
- Nếu đốt hiđrocacbon thu được nCO2 < nH2O ⇒ Hiđrocacbon đem đốt là ankan (CnH2n+2).
- Trong điều kiện thiếu oxi ngoài CO2 và H2O phản ứng còn tạo CO, muội than gây hại cho môi trường.
- Nếu có xúc tác và to thích hợp, ankan bị oxi hóa không hoàn toàn tạo thành dẫn xuất chứa oxi.
Ứng dụng và điều chế của ankan
Ứng dụng của ankan
- Dùng làm nhiên liệu trong hàn cắt kim loại.
- Dùng làm dầu bôi trơn, dung môi.
- Để tổng hợp nhiều chất hữu cơ khác: CH3Cl, CH2Cl2, CCl4, CF2Cl2, …
- Đặc biệt từ CH4 điều chế được nhiều chất khác nhau: hỗn hợp CO + H2, ammoniac, C2H2, rượu metylic, andehit fomic, …
Điều chế của ankan
+) Điều chế metan
Các nguồn khí: từ khí thiên nhiên, khí hồ ao, khí dầu mỏ, khí chưng than đá.
Tổng hợp:
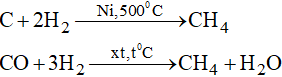
Từ khí CH3COONa khan:
![]()
Từ Nhôm cacbua (Al4C3):
Al4C3 + 12H2O → 4Al(OH)3↓ + 3CH4↑
+) Điều chế các ankan khác:
- Lấy từ các nguồn thiên nhiên: Khí dầu mỏ, khí thiên nhiên, sản phẩm cracking.
- Từ các muối axit hữu cơ:
![]()
Các dạng bài tập ankan thường gặp
Bài 1: Chất khí A là 1 xicloankan. Khi đốt cháy 672 ml A(đktc), thì thấy khối lượng CO2 tạo thành nhiều hơn khối lượng nước tạo thành 3,12 g.
a. Xác định công thức phân tử.
b. Viết công thức cấu tạo và tên các xicloankan ứng với công thức phân tử tìm được.
c. Cho chất A qua dung dịch brom, màu của dung dịch mất đi. Xác định công thức cấu tạo đúng của chất A.
Giải:
Số mol khí A là: nA = 0,672/22,4 = 0,03 mol; đốt cháy xicloankan: nCO2 = nH2O = x
Khối lượng CO2 lớn hơn khối lượng H2O là 3,12 gam: mCO2 – mH2O = 44x – 18x = 26x = 3,12 ⇒ x = 0,12 mol.
a. Phương trình đốt cháy:
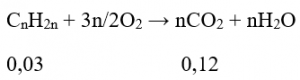
n = 0,12/0,03 = 4
Vậy CTPT của xicloankan là: C4H8
b. Các đồng phân cấu tạo xicloankan của C4H8 là:
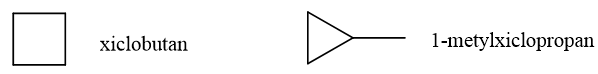
c. Chất A làm mất màu dung dịch nước brom. Vậy CTCT của A là
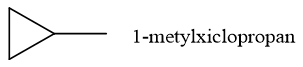
Bài 2: Đốt cháy hoàn toàn một xicloankan A thu được hỗn hợp khí và hơi. Dẫn toàn bộ hỗn hợp đó qua bình đựng dung dịch Ba(OH)2 dư thấy tạo ra 9,85 gam kết tủa. Khối lượng dung dịch sau phản ứng tăng hay giảm bao nhiêu gam?
Giải:
nH2O = nCO2 = nBaCO3 = 9,85/197 = 0,05 mol ⇒ mH2O = 0,05.18 = 0,9 gam; mCO2 = 0,05.44 = 2,2 gam; mgiảm= 9,85 – (0,9 + 2,2) = 6,75.
Bài 3 : Hỗn hợp khí A chứa một ankan và một monoxicloankan. Tỉ khối của A đối với hiđro là 25,8. Đốt cháy hoàn toàn 2,58 g A rồi hấp thụ hết sản phẩm cháy vào dung dịch Ba(OH)2 dư, thu được 35,46 g kết tủa. Công thức phân tử của các chất trong hỗn hợp A là
Giải:
nCO2 = nBaCO3 = 35,46/197 = 0,18 mol; nA= 2,58/51,6 = 0,05 mol; mH = 2,58 – 0,18.12 = 0,42 gam ⇒ nH2O = 0,21 mol; nankan = 0,21 – 0,18 = 0,03 mol ⇒ nxicloankan = 0,02 mol;
CTPT của ankan và xicloankan lần lượt là: CnH2n+2 và CmH2m; ta có: 0,02n + 0,03m = 0,18 ⇔ 2n + 3m = 18 ⇒ n = 3 và m = 4.
Bài 4: Hỗn hợp B gồm một ankan và 1 xicloankan. Dẫn m g B qua bình chứa nước brom dư thì khối lượng bình tăng 4,2 gam. Đốt cháy hoàn toàn m gam B thu được 11,2 lit CO2 (đktc) và 10,8 gam H2O. Thành phần % khối lượng ankan trong B là?
Giải:
Khối lượng bình brom tăng là khối lượng của xicloankan: mxicloankan = 4,2 gam
nH2O = 10,8/18 = 0,6 mol; nCO2 = 11,2/22,4 = 0,5 mol
mB = mC + mH = 0,5.12 + 0,6.2 = 7,2 gam
⇒ mankan = 7,2 – 4,2 = 3 gam
⇒ %(m)ankan = 3.110%/7,2 = 41,67%
Bài 5: Xicloankan (chỉ có một vòng) A có tỉ khối so với nitơ bằng 3. A tác dụng với clo có chiếu sáng chỉ cho một dẫn xuất monoclo duy nhất, xác định công thức cấu tạo cuả A?
Giải:
MA = 3.28 = 84 = 14n ⇒ n = 6
Bài 6: Crackinh butan thu được 35 mol hh A gồm CH4, C2H6, H2, C2H4, C3H6, C4H8 và C4H10 dư. Dẫn A lội qua bình nước brom dư thấy có 20 mol khí đi ra khỏi bình (biết rằng chỉ có C2H4, C3H6, C4H8 phản ứng với Br2 và đều theo tỉ lệ số mol 1:1). Nếu đốt cháy hoàn toàn A thì thu được a mol CO2.
a. Tính hiệu suất phản ứng tạo hh A.
b. Tính giá trị của a.
Giải:
a. Phương trình phản ứng:
C4H10 −tº, xt→ CH4 + C3H6
C4H10 −tº, xt→ C2H6 + C2H4
C4H10 −tº, xt→ H2 + C4H8
Số mol anken thu được: nanken= 35 – 20 = 15mol
Số mol butan ban đầu là: nđ = nbutan = ns – nanken = 35 – 15 = 20 mol
Hiệu suất cracking butan là H = (ns– nđ)/nđ .100% = (35-20)/20.100% = 75%
b Đốt cháy hỗn hợp A là đốt chay butan:
C4H10 + 11/2O2 → 4CO2 + 5H2O
20 80 mol
Vậy số mol CO2 thu được khi đốt cháy hỗn hợp A là 80 mol
Bài 7: Nung một lượng butan trong bình kín (cố xúc tác thích hợp) thu được hỗn hợp X gồm ankan và anken. Tỉ khối của X so với khí hiđro là 21,75. Thành phần phần trăm thể tích của butan trong X là:
Giải:
MX = 21,75.2 = 43,5. Chọn số mol hỗn hợp X là 1 mol
C4H10 → CnH2n+2 + CmH2m
a mol a mol a mol
BTKL:
⇒ a = 1 – 0,75 = 0,25 mol ⇒ C4H10 còn dư: 0,75 – 0,25 = 0,5 mol
⇒ % thể tích C4H10 trong X là 50%
Mong rằng những nội dung trên đây sẽ giúp bạn trả lời được những thắc mắc câu hỏi của mình. Hơn hết đó là có thể giải được những bài toán của mình